
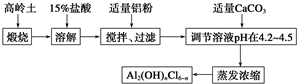
分析 加入鹽酸,二氧化硅不反應,Al2O3、Fe2O3與鹽酸反應生成氯化鋁、氯化鐵,加入適量鋁粉,過濾,除去溶液中的鐵離子,在濾液中加入適量碳酸鈣調節pH在4.2~4.5,將溶液蒸發濃縮,可得到[Al2(OH)nCl6-n],以此解答該題.
解答 解:加入鹽酸,二氧化硅不反應,Al2O3、Fe2O3與鹽酸反應生成氯化鋁、氯化鐵,加入適量鋁粉,過濾,除去溶液中的鐵離子,在濾液中加入適量碳酸鈣調節pH在4.2~4.5,將溶液蒸發濃縮,可得到[Al2(OH)nCl6-n],
(1)“溶解”過程反應的離子方程式有 Al2O3+6H+=2Al3++3H2O、Fe2O3+6H+=2Fe3++3H2O,故答案為:Al2O3+6H+=2Al3++3H2O、Fe2O3+6H+=2Fe3++3H2O;
(2)鋁可與鐵離子反應生成亞鐵離子,鋁與亞鐵離子反應置換出鐵,加入鋁粉最主要作用是:除去溶液中的鐵元素,故答案為:除去溶液中的鐵元素;
(3)將濾液3的pH調至4.2~4.5,利用水解反應得到液體聚合氯化鋁,防止生成氫氧化鋁沉淀,實驗時pH超過4.5,Al3+會形成Al(OH)3沉淀;pH低于4.2,Al3+水解程度很小,很難形成液態堿式氯化鋁[Al2(OH)nCl6-n],
故答案為:pH超過4.5,Al3+會形成Al(OH)3沉淀;pH低于4.2,Al3+水解程度很小,很難形成液態堿式氯化鋁[Al2(OH)nCl6-n];
(4)控制該溫度在一定范圍之間,可水浴加熱,氯化鋁水解生成Al2(OH)nCl6-n,反應的化學方程式為2AlCl3+nH2O═Al2(OH)nCl6-n+nHCl,
故答案為:水浴加熱;2AlCl3+nH2O═Al2(OH)nCl6-n+nHCl.
點評 本題考查了物質制備方法和實驗探究,為高頻考點,掌握實驗基本操作和理解實驗原理是解題關鍵,題目難度中等,需要學生具備扎實的基礎,難度中等.


 怎樣學好牛津英語系列答案
怎樣學好牛津英語系列答案科目:高中化學 來源: 題型:選擇題
| A. | Al3+、ClO-、Cl- | B. | Na+、NH4+、Cl- | C. | Mg2+、Cl-、Fe2+ | D. | Mg2+、Ba2+、Br- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
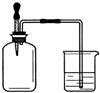 如右圖所示,集氣瓶 內充滿某混合氣體,置于光亮處,將滴管內的水擠入集氣瓶后,燒杯中的水會進入集氣瓶,集氣瓶內氣體是( )
如右圖所示,集氣瓶 內充滿某混合氣體,置于光亮處,將滴管內的水擠入集氣瓶后,燒杯中的水會進入集氣瓶,集氣瓶內氣體是( )| A. | ①② | B. | ②④ | C. | ②③ | D. | ③④ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
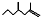 (2,4-二甲基-1-庚烯),
(2,4-二甲基-1-庚烯),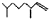 (3,7-二甲基-1-辛烯),家蠶的性信息素為:CH3(CH2)3CH=CH-CH=CH(CH2)3CH3.下列說法正確的是( )
(3,7-二甲基-1-辛烯),家蠶的性信息素為:CH3(CH2)3CH=CH-CH=CH(CH2)3CH3.下列說法正確的是( )| A. | 以上三種信息素互為同系物 | |
| B. | 以上三種信息素均能使溴的四氯化碳溶液褪色 | |
| C. | 2,4-二甲基-1-庚烯與3,7-二甲基-1-辛烯互為同分異構體 | |
| D. | 家蠶的性信息素與1molBr2加成產物只有一種 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
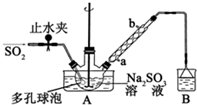 次硫酸氫鈉甲醛(NaHSO2•HCHO•2H2O)俗稱吊白塊,不穩定,120℃時會分解,在印染、醫藥以及原子能工業中有廣泛應用.以Na2SO3、SO2、HCHO和鋅粉為原料制備次硫酸氫鈉甲醛的實驗步驟如圖:
次硫酸氫鈉甲醛(NaHSO2•HCHO•2H2O)俗稱吊白塊,不穩定,120℃時會分解,在印染、醫藥以及原子能工業中有廣泛應用.以Na2SO3、SO2、HCHO和鋅粉為原料制備次硫酸氫鈉甲醛的實驗步驟如圖:查看答案和解析>>
科目:高中化學 來源: 題型:填空題
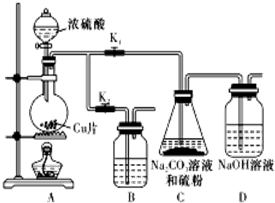 硫代硫酸鈉(Na2S2O3)可由亞硫酸鈉和硫粉通過化合反應制得.已知:Na2S2O3在酸性溶液中不能穩定存在.
硫代硫酸鈉(Na2S2O3)可由亞硫酸鈉和硫粉通過化合反應制得.已知:Na2S2O3在酸性溶液中不能穩定存在.| 編號 | 1 | 2 | 3 | 4 |
| 溶液的體積/mL | 10.00 | 10.00 | 10.00 | 10.00 |
| 消耗I2標準溶液的體積/mL | 19.99 | 19.98 | 17.13 | 20.03 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 弱酸化學式 | CH3COOH | HCN | H2CO3 |
| 電離平衡常數(25℃) | 1.8×l0-5 | 4.9×l0-10 | K1=4.3×l0-7K2=5.6×l0-11 |
| A. | 向NaCN 溶液中通入少量CO2發生的離子反應為:2CN-+H2O+CO2═2HCN+CO32- | |
| B. | 等物質的量濃度的各溶液pH關系為:pH(NaCN)>pH(Na2CO3)>pH(CH3COONa) | |
| C. | a mol/LHCN溶液與b mol/LNaOH溶液等體積混合后,所得溶液中c(Na+)>c(CN-),則b一定大 于a | |
| D. | NaHCO3和Na2CO3的混合溶液中,一定存在:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1mol KClO3 參加反應有2mol電子轉移 | |
| B. | ClO2是氧化產物 | |
| C. | H2C2O4的氧化性強于ClO2的氧化性 | |
| D. | KClO3 在反應中得到電子,作氧化劑 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com