
分析 (1)硫酸鋁是強酸弱堿鹽,鋁離子水解導致溶液呈酸性;
(2)在酸溶液中,氫離子幾乎全部來自于酸的電離,而氫氧根全部來自于水的電離;
在鹽溶液中,氫離子和氫氧根均全部來自于水的電離;
(3)醋酸根離子水解,溶液顯堿性.
解答 解:(1)硫酸鋁是強酸弱堿鹽,鋁離子水解導致溶液呈酸性,水解方程式為Al3++3H2O?Al(OH)3+3H+,故答案為:酸;Al3++3H2O?Al(OH)3+3H+;
(2)25℃下,pH=5的鹽酸溶液中c(H+)=10-5mol/L,c(OH-)=10-9mol/L,而在酸溶液中,氫離子幾乎全部來自于酸的電離,而氫氧根全部來自于水的電離,故由水電離出的c(H+)=c(OH-)=10-9mol/L;
25℃下,pH=5的氯化銨溶液中,c(H+)=10-5mol/L,c(OH-)=10-9mol/L,但在氯化銨溶液中,氫離子和氫氧根均全部來自于水的電離,但由于銨根離子水解將部分氫氧根結合,故溶液中的氫離子是水電離出的全部,故由水電離出的c(H+)=c(OH-)=10-5mol/L;
故答案為:10-9mol/L;10-5mol/L;
(3)醋酸根離子水解,溶液顯堿性,顯性離子大于隱性離子,則離子關系為c(Na+)>c(CH3COO-)>c(OH-)>c(H+),故答案為:c(Na+)>c(CH3COO-)>c(OH-)>c(H+).
點評 本題考查酸堿溶液的混合、涉及電離、水解等,注重高考常考考點的考查,側重反應原理的訓練,題目難度中等.


科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 自來水廠用含鐵的化合物作凈水劑 | |
| B. | 用丁達爾效應區分氫氧化鐵膠體和氯化鐵溶液 | |
| C. | 一束平行光照射蛋白質溶液時,從側面要看到光亮的通路 | |
| D. | 在三氯化鐵溶液中滴入氫氧化鈉溶液出現紅褐色沉淀 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 質子數為17、中子數為20的氯(Cl)原子:${\;}_{17}^{20}$Cl | |
| B. | CO2電子式: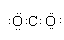 | |
| C. | 鎂離子的結構示意圖: | |
| D. | CCl4分子的比例模型: |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com