
分析 3Cu+8HNO3(稀)=3Cu(NO3)2+4H2O+2NO↑中,Cu元素的化合價由0升高為+2價,N元素的化合價由+5價降低為+2價,以此來解答.
解答 解:3Cu+8HNO3(稀)=3Cu(NO3)2+4H2O+2NO↑中,Cu元素的化合價升高,則Cu為還原劑,N元素的化合價降低,被還原,則NO為還原產物;有11.2L(標準狀況)NO氣體生成,轉移電子為$\frac{11.2L}{22.4L/mol}$×(5-3)×NA=1.5NA,該反應的離子反應為3Cu+8H++2NO3-=3Cu2++2NO↑+H2O,
故答案為:Cu;NO;1.5NA;3Cu+8H++2NO3-=3Cu2++2NO↑+H2O.
點評 本題考查氧化還原反應,為高頻考點,把握反應中元素的化合價變化為解答的關鍵,側重氧化還原反應基本概念及轉移電子的考查,題目難度不大.


 計算高手系列答案
計算高手系列答案科目:高中化學 來源: 題型:選擇題
| A. | 膠體區別于其他分散系的本質特征是丁達爾現象 | |
| B. | 將飽和FeCl3溶液逐滴加入NaOH溶液中可制備Fe(OH)3膠體 | |
| C. | Al(OH)3膠體能使水中的懸浮顆粒沉降,達到凈水的目的 | |
| D. | 豆漿、蔗糖溶液均屬于膠體 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
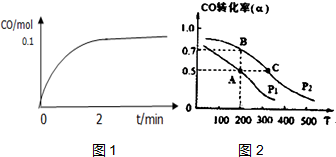 工業上一般以CO和H2為原料合成甲醇,該反應的熱化學方程式為:CO (g)+2H2 (g)?CH3OH (g)△H=-116kJ/mol
工業上一般以CO和H2為原料合成甲醇,該反應的熱化學方程式為:CO (g)+2H2 (g)?CH3OH (g)△H=-116kJ/mol查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 抗酸藥能中和胃里過多的鹽酸,緩解胃部不適,是一類治療胃痛的藥 | |
| B. | 碳酸鈣、氫氧化鋁都能制成抗酸藥 | |
| C. | 青霉素有阻止多種細菌生長的優異功能,雖經1×107 倍稀釋,仍有療效 | |
| D. | 中草藥麻黃堿可用于治療失眠、多夢等癥狀 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氫氧化銅和鹽酸、氫氧化鋇和鹽酸 | |
| B. | 氯化鋇和硫酸鉀、氫氧化鋇和硫酸 | |
| C. | 澄清石灰水和碳酸鈉、氯化鈣和碳酸鉀 | |
| D. | 碳酸氫鈉和硫酸、碳酸鈉和鹽酸 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 加入足量鎂粉的Fe2(SO)3溶液 | |
| B. | FeCl2溶液與稀硝酸混合后的溶液 | |
| C. | 鐵絲在足量的氯氣中燃燒后所得產物的溶液 | |
| D. | 長期暴露在空氣中的綠礬溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
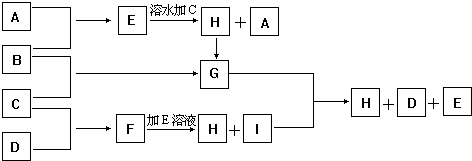
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 炭具有強還原性,高溫下能將二氧化硅還原為硅 | |
| B. | Na的金屬性比Mg強,可用Na與MgCl2溶液反應制取金屬Mg | |
| C. | 光照時乙烷和氯氣能發生取代反應,工業上常用該反應生產氯乙烷 | |
| D. | 二氧化錳具有強氧化性,能將雙氧水氧化為氧氣 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com