
已知某氣體反應的平衡常數可表示為K=c(CH3OCH3)c(H2O)/[c(CH3OH)]2,該反應在不同溫度下的平衡常數:400℃,K=32;500℃,K=44.
請回答下列問題:
(1)寫出上述反應的化學方程式 .
(2)該反應的正反應是 反應(填“放熱”或者“吸熱”)
(3)已知在密閉容器中,測得某時刻各組分的濃度如下:

①此時系統溫度400℃,比較正、逆反應速率的大小:v正 v逆 (填“>”、“<”或“=”).
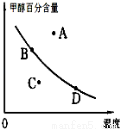
②若以甲醇百分含量為縱坐標,以溫度為橫坐標,此時反應點在圖象的位置是圖中 點.比較圖中B、D兩點所對應的正反應速率B D(填“>”、“<”或 “=”).理由是 .
(4)一定條件下要提高反應物的轉化率,可以采用的措施是
a.升高溫度 b.加入催化劑
c.壓縮容器的體積 d.增加水蒸氣的濃度
e.及時分離出產物.
 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源:2015-2016學年廣西省高二上段考文化學試卷(解析版) 題型:填空題
在氮的單質和化合物中,遇到HCl會產生白煙的是 (用字母填空);與氫氧化鈣加熱發生反應產生刺激性氣味氣體的是 (用字母填空)。
A.氮氣 B.氨氣 C.硝酸鈉 D.氯化銨
查看答案和解析>>
科目:高中化學 來源:2015-2016學年黑龍江省高二上期末考試化學試卷(解析版) 題型:填空題
(1)甲醇(CH3OH)是重要的能源物質,研究甲醇具有重要意義。為提高甲醇燃料的利用率,科學家發明了一種燃料電池,電池的一個電極通入空氣,另一個電極通入甲醇氣體,電解質是摻入了Y2O3的ZrO2晶體,在高溫下它能傳導O2-。電池工作時正極反應式為 。
若以該電池為電源,用石墨做電極電解100 mL含有如下離子的溶液。
離子 | Cu2+ | H+ | Cl- | SO42- |
c/mol·L-1 | 1 | 4 | 4 | 1 |
電解一段時間后,當兩極收集到相同體積(相同條件)的氣體時(忽略溶液體積的變化及電極產物可能存在的溶解現象),陽極上收集到氧氣標況下的體積為 L。
(2)甲醇對水質會造成一定的污染,有一種電化學法可消除這種污染,其原理是:通電后將Co2+氧化成Co3+,然后以Co3+做氧化劑把水中的甲醇氧化成CO2而凈化。實驗室用右圖裝置模擬上述過程:
①寫出陽極電極反應式 ;
②除去甲醇的離子反應為 ,該過程中被氧化的元素是_____ ,當產生標準狀況下2.24 L CO2時,共轉移電子 mol。
查看答案和解析>>
科目:高中化學 來源:2015-2016學年黑龍江省高二上期末考試化學試卷(解析版) 題型:選擇題
25℃時,下列各組離子在特定溶液中一定能大量共存的是( )
A.由水電離的c(H+)=1×10﹣14mol•L﹣1的溶液中:Ca2+、K+、Cl﹣、HCO3﹣
B.甲基橙呈紅色的溶液:NH4+、Ba2+、AlO2﹣、Cl﹣
C.在pH=0的溶液中:Na+、NO3﹣、SO32﹣、K+
D.pH=12的溶液:K+、Na+、CH3COO﹣、Br﹣
查看答案和解析>>
科目:高中化學 來源:2015-2016學年山西省高二上12月月考化學試卷(解析版) 題型:填空題
甲醇是人們開發和利用的一種新能源。已知:
①2H2(g)+O2(g)===2H2O(l) ΔH1=-571.8kJ/mol;
②CH3OH(g)+1/2O2(g)===CO2(g)+2H2(g) ΔH2=-192.9kJ/mol
(1)甲醇蒸氣完全燃燒的熱化學方程式為_____________________________。
(2)反應②中的能量變化如圖所示,則ΔH2=_________________________。
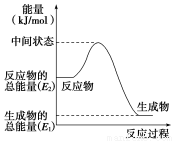
(3)H2(g)的燃燒熱為____________________。
查看答案和解析>>
科目:高中化學 來源:2015-2016年陜西西藏民族學院附屬中學高二上期末化學卷(解析版) 題型:選擇題
某可逆反應過程的能量變化如圖所示,下列說法正確的是( )
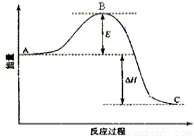
A.該反應過程為吸熱反應
B.若加入催化劑,B點會降低
C.若加入催化劑,△H數值會減小
D.若升高溫度,則平衡向正反應方向移動
查看答案和解析>>
科目:高中化學 來源:2016屆吉林省高三上期末考試化學試卷(解析版) 題型:選擇題
短周期元素X、Y、Z、W、U原子序數依次遞增。X與W位于同一主族,Z元素的單質既能與鹽酸反應也能與NaOH溶液反應,W原子的最外層電子數是次外層電子數的一半,Z、W、U原子的最外層電子數之和為13。Y元素的單質在X的某種氧化物中可燃。下列說法正確的是
A.X、W、U的最高價氧化物對應的水化物酸性由強到弱的順序為:U>W>X
B.Y、Z元素的單質作電極,在NaOH溶液中構成原電池,Z電極上產生大量氣泡
C.Y、Z、U元素的簡單離子半徑由大到小的順序:Y>Z>U
D.室溫下,0.05 mol/L U的氣態氫化物的水溶液的pH>1
查看答案和解析>>
科目:高中化學 來源:2015-2016學年吉林省高二上期末考試化學試卷(解析版) 題型:選擇題
下列敘述正確的是
A.0.1 mol/LCH3COONa溶液中:c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
B.Na2CO3溶液加水稀釋后,恢復至原溫度,pH和Kw均減小
C.pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,c(H+)不相等
D.在Na2S溶液中加入AgCl固體,溶液中c(S2-)下降
查看答案和解析>>
科目:高中化學 來源:2016屆陜西省高三上期末化學試卷(解析版) 題型:選擇題
某溫度下,飽和石灰水的溶解度為Sg,密度為ρg/mL,向足量該飽和溶液中加入mgCaO,充分作用后,恢復到原來溫度,下列有關說法不正確的是( )
A.最終得到沉淀的質量大于 37m/28g
B.該飽和溶液質量百分比濃度為 s/(100+s)%
C.最終所得溶液PH不變
D.該飽和溶液中溶質物質的量濃度為
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com