
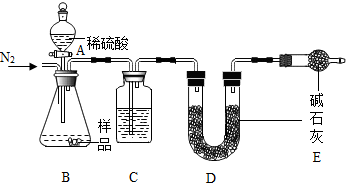
分析 (1)根據NaHCO3俗稱為小蘇打解答,根據堿石灰會吸收水分和二氧化碳進行分析;
(2)根據E的作用是防止空氣中的水和二氧化碳進入D解答;
(3)根據堿石灰是堿性干燥劑,鹽酸具有揮發性進行分析;
(4)根據實驗時需要重復“加熱、冷卻、稱量”操作多次,可以使碳酸氫鈉完全分解進行分析;
(5)根據根據題目中的信息,寫出NaHCO3完全分解的化學方程式解答;
(6)根據實驗過程中減少的質量是水和二氧化碳的質量進行分析.
解答 解:
(1)NaHCO3俗稱為小蘇打;堿石灰會吸收水分和二氧化碳,實驗在用堿石灰吸收二氧化碳之前,需要將氣體干燥,C中盛放的物質是濃硫酸;
(2)E的作用是防止空氣中的水和二氧化碳進入D,否則,若無裝置E,在其他操作正確的情況下,不能準確測定樣品中NaHCO3的質量分數,使測定結果偏大;
(3)堿石灰是堿性干燥劑,鹽酸具有揮發性,會對所測數據造成影響,所以不能準確測定樣品中NaHCO3的質量分數;
(4)實驗時需要重復“加熱、冷卻、稱量”操作多次,可以使碳酸氫鈉完全分解;
(5)NaHCO3完全分解的化學方程式為:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑;
(6)實驗過程中減少的質量是水和二氧化碳的質量,固體減少質量為:41.2g-35g=6.2g;
設樣品中含有碳酸氫鈉為x,
2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑ 固體減少
168 62
x 6.2g
$\frac{168}{x}=\frac{62}{6.2g}$
x=16.8g
樣品中碳酸氫鈉為:41.2g-21.2g=20g
所以樣品中NaHCO3的質量分數為:$\frac{16.8g}{20g}$×100%=84%.
答案:
(1)小蘇打; 濃硫酸;
(2)不能;
(3)鹽酸具有揮發性,D中的堿石灰既吸收生成的CO2,還會吸收揮發出的HCl氣體,使測定結果偏大;
(4)使碳酸氫鈉完全分解;
(5)2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑;
(6)樣品中NaHCO3的質量分數為84%.
點評 本題考查了碳酸鈉的性質以及有關的計算,完成此題,可以依據已有的知識進行.


 波波熊暑假作業江西人民出版社系列答案
波波熊暑假作業江西人民出版社系列答案 學而優暑期銜接南京大學出版社系列答案
學而優暑期銜接南京大學出版社系列答案 Happy holiday歡樂假期暑假作業廣東人民出版社系列答案
Happy holiday歡樂假期暑假作業廣東人民出版社系列答案科目:初中化學 來源: 題型:實驗探究題
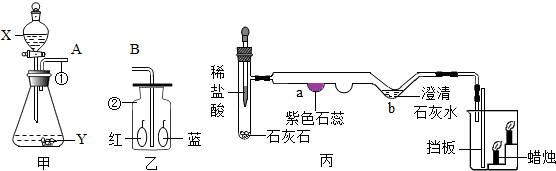
查看答案和解析>>
科目:初中化學 來源: 題型:推斷題
 鈣元素對人類生命和生活具有重要意義.
鈣元素對人類生命和生活具有重要意義.查看答案和解析>>
科目:初中化學 來源: 題型:推斷題
 A、B、C、D、E是初中化學常見的不同類別物質(單質、氧化物、酸、堿和鹽),它們之間相互關系如圖(“→”表示反應轉化關系,“-”表示相互之間能反應,部分反應物、生成物以及反應條件省略).若往D、E兩種溶液中分別滴入紫色石蕊試液,溶液均顯藍色;D與E兩種溶液混合有白色沉淀產生;C與E的溶液反應有氣泡產生,該氣體能使澄清石灰水變渾濁.請回答下列問題:
A、B、C、D、E是初中化學常見的不同類別物質(單質、氧化物、酸、堿和鹽),它們之間相互關系如圖(“→”表示反應轉化關系,“-”表示相互之間能反應,部分反應物、生成物以及反應條件省略).若往D、E兩種溶液中分別滴入紫色石蕊試液,溶液均顯藍色;D與E兩種溶液混合有白色沉淀產生;C與E的溶液反應有氣泡產生,該氣體能使澄清石灰水變渾濁.請回答下列問題:查看答案和解析>>
科目:初中化學 來源: 題型:推斷題
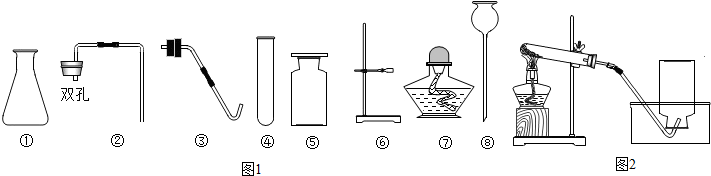
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
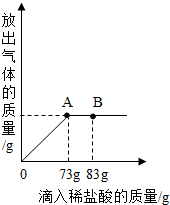 將碳酸鈉和氯化鈉的混合物加足量水溶解,制成131.4克溶液.向其中逐漸滴加溶質質量分數為10%的稀鹽酸,放出氣體的總質量與所滴入稀鹽酸的質量關系曲線如圖所示.當滴加稀鹽酸至圖中B點時,將溶液倒入蒸發皿中蒸發,最終稱得固體的質量為25.6克.請根據題意回答問題:
將碳酸鈉和氯化鈉的混合物加足量水溶解,制成131.4克溶液.向其中逐漸滴加溶質質量分數為10%的稀鹽酸,放出氣體的總質量與所滴入稀鹽酸的質量關系曲線如圖所示.當滴加稀鹽酸至圖中B點時,將溶液倒入蒸發皿中蒸發,最終稱得固體的質量為25.6克.請根據題意回答問題:查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com