
實驗室用大理石與稀鹽酸反應制取C02,反應后所得溶
液體積為40 mL(假設大理石中的雜質不與鹽酸反應,反應
前后溶液體積不變)。向該溶液中勻速逐滴加入Na2C03溶液
并不斷攪拌,測得溶液的pH隨時間變化如圖所示,該過程
共放出氣體660 mL(密度為2.0 g/L),析出沉淀5.090
(1) 根據圖像可以看出,Na2C03首先與溶液中的 反應。
(2)本實驗制取CO2所用大理石中含CaC03 g。
(3)已知制取C02所用稀鹽酸的密度為1.06 g/cm3,求這種鹽酸的質量分數。(計算結果保留1位小數,無計算過程不給分)
【答案】(1)HCl(或鹽酸)(2)5.0
(3)解:設制取二氧化碳時,與大理石反應的HCl的質量為x,剩余HCl的質量為y
CaCO3 + 2HCl === CaCl2 + H2O + CO2↑
100 73
5.0g x
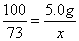
解得:x=3.65g(1分)
Na2CO3 + 2HCl === 2NaCl + H2O + CO2↑
73 44
y 0.66L 2g/L
2g/L
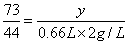
解得:y=2.19g
鹽酸的溶質質量分數為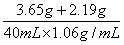
 100%=13.8%
100%=13.8%
【解析】(1)從圖中,開始時溶液的pH迅速增大,可知,開始時,碳酸鈉與鹽酸反應;(2)根據質量守恒定律,生成的沉淀是碳酸鈉與氯化鈣反應所得,反應前后鈣元素的質量不變,故生成的沉淀即為原大理石中碳酸鈣的質量;(3)利用二氧化碳的質量可計算出與碳酸鈉反應的稀鹽酸的質量,利用碳酸鈣的質量可計算出與與大理石反應的鹽酸的質量,兩部分鹽酸的質量和除以溶液的質量即為鹽酸的質量分數。


科目:初中化學 來源: 題型:
我國大部分地區深受酸雨的危害,煤燃燒產生的SO2是形成酸雨的主要污染物,SO2與水結合生成弱酸性亞硫酸(H2SO3)。
已知:H2SO3易分解生成水和SO2,也易與空氣中的氧氣或稀硝酸反應生成H2SO4;H2SO3和SO2都能使紅色的品紅溶液褪色。
(1)酸雨是pH小于________的降雨。
(2)常用脫硫方法減少廢氣中的SO2,以生石灰(CaO)為脫硫劑,高溫下與廢氣中的SO2與O2化合生成CaSO4,化學方程式為:__________________________________。
(3)實驗室常用亞硫酸鹽與HCl(或H2SO4)反應制備SO2,Na2SO3與鹽酸反應的化學方程式:____________________________。
(4)小鴻同學利用中和反應的原理,在空氣中放置一段時間的酸雨(pH約為3)中加入足量的KOH,并就反應后混合溶液中的鹽成分進行探究:
【提出猜想】反應后的混合溶液中鹽的成分是什么?
【進行猜想】猜想1:只有K2SO3;猜想2:____________;猜想3:既有K2SO4,也有K2SO3。
【實驗探究】限選試劑:稀硫酸、稀鹽酸、稀硝酸、氯化鋇溶液、澄清石灰水、品紅溶液、紫色石蕊溶液。
| 步驟 | 實驗操作 | 預期現象與結論 |
| 1 | 各取2 mL反應后的混合溶液分別加入A、B兩支試管 | — |
| 2 | 向A試管中滴加足量的稀硫酸,隨即滴入幾滴紅色品紅溶液 | __________________________________________,證明含有K2SO3 |
| 3 | 向B試管中加入__________,再加入足量的__________ | 先有白色沉淀,后有氣體產生,沉淀部分溶解,證明含有K2SO4,即猜想3成立 |
查看答案和解析>>
科目:初中化學 來源: 題型:
生活中常用到各種干燥劑(能除去潮濕物質中水分的物質)。
(1)硅膠是無色或白色顆粒,其主要成分是SiO2,其中Si元素的化合價為_____。
(2)生石灰是白色塊狀固體,吸水后變成粉末,該反應的化學方程式是_____,該反應可用于自發熱飯盒的原因是______。
(3)分子篩干燥劑是鋁硅酸鹽化合物,其晶體結構中有規整而均勻的孔道,只允許直徑比孔徑小的分子進入,能吸附水氣和其 它氣體,吸濕速度極快。分子篩干燥劑吸水前后的變化屬于______變化(填“物理”或“化學”)。
它氣體,吸濕速度極快。分子篩干燥劑吸水前后的變化屬于______變化(填“物理”或“化學”)。
(4)“雙吸劑”的主要成分是還原鐵粉,常用于食品保鮮,其原因是______。
查看答案和解析>>
科目:初中化學 來源: 題型:
人體注射葡萄糖溶液可以補充能量,葡萄糖(C6H12O6)在體內經緩慢氧化生成二氧化碳和水,釋放出能量。若1 000克5%葡萄糖注射液中的葡萄糖完全氧化,計算:
(1)理論上至少消耗O2多少克?
(2)多少升空氣中含有這些質量的氧氣?
(相對原子質量:H:1、C:12、O:16、O2密度按1.43克/升計,計算結果取整數)
查看答案和解析>>
科目:初中化學 來源: 題型:
現有9.3g NaOH與Na2CO3的固體混合物,測得其中鈉元素與碳元素的質量比為23:3。在室溫下,將該混合物與50g稀硫酸混合,恰好完全反應,所得不飽和溶液的質量為57.1g,則原固體混合物中含有鈉元素的質量為下列的( )
A.1.15g
B.2.3g
C.4.6g
D.6.9g
查看答案和解析>>
科目:初中化學 來源: 題型:
下圖表示金屬活動性順序中銅、鐵和鋁被人類大規模開發、利用的大致年限。

(1)分析改圖的規律,你認為金屬被大規模開發、利用的先后順序主要與 有關。
(2)科學小組的同學對模擬濕法煉銅實驗中得到的鐵、銅固體混合物進行含量測定,稱取10克固體混合物置于燒杯中,滴加一定質量分數的稀硫酸溶液,記錄并繪制了如圖所示的曲線。
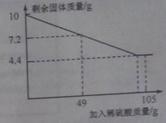
①10克固體混合物中銅的質量為 克;
②所用稀硫酸溶液溶質的質量分數是多少?(寫出計算過程)
查看答案和解析>>
科目:初中化學 來源: 題型:
小英同學為了側定某地區石灰石樣品中碳酸鈣的質量分數,取該樣品15g,現將75m1的稀鹽酸分三次加人石灰石樣品中,每次充分反應后測得生成氣體的質量,實驗數據如下表:
| 實驗 | 第一次 | 第二次 | 第三次 |
| 加人稀鹽酸的量/ml | 25 | 25 | 25 |
| 生成氣體的質量/g | 2.2 | m | 1.1 |
試求:
(1)m的值是 g。
(2)求該樣品中碳酸鈣的質量分數(保留一位小數)?
查看答案和解析>>
科目:初中化學 來源: 題型:
某混合物中含有碳酸鈣和氯化鈣,取該混合物6g,向其中加入一定質量的質量分數為10%的稀鹽酸,恰好完全反應,產生2.2g氣體。(假設氣體全部逸出)。
計算:
(1) 所取混合物中碳酸鈣的質量。
(2) 所加稀鹽酸的質量
(3) 反應后所得溶液中的質量分數(計算結果精確到0.1%)
查看答案和解析>>
科目:初中化學 來源: 題型:
硫酸是化工生產中重要的酸,其產量最大,用途最廣,消耗量最多。歷史上曾將硫酸的產量或消耗量作為一個國家化工生產發達程度的標志。
濃硫酸具有吸水性、脫水性和強氧化性。濃硫酸的腐蝕性主要是由它的脫水性和強氧化性引起的。稀硫酸有強酸性,稀硫酸的腐蝕性則主要是由酸性及水分蒸發后變濃而產生的。
 硫酸的用途極廣,常用于生產化肥、冶煉金屬、農藥、制藥等。
硫酸的用途極廣,常用于生產化肥、冶煉金屬、農藥、制藥等。
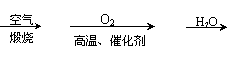
工業制硫酸的流程為:FeS2 SO2 SO2 H2SO4
(1)綜合分析以上材料,并結合已有知識,請回答:
①工業制H2SO4可能會引起的環境問題是 。
②在實驗室中不慎將濃硫酸 沾到皮膚上的處理方法是 。
沾到皮膚上的處理方法是 。
A.立即用大量水沖洗,然后再涂上3%~5%的碳酸氫鈉溶液。
B.立即用稀氫氧化鈉溶液沖洗,然后再用水沖洗。
(2)某工廠化驗室用9.8%的稀硫酸洗滌一定量化工產品中殘留Ba(OH)2,當消耗稀硫酸100g時,沉淀不再產生,問此時液體的pH= 7 (不考慮其它物質的影響),求化工產品中殘留Ba(OH)2的質量。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com