
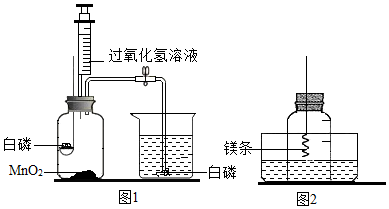
分析 實驗一:根據燃燒的條件分析;燃燒的條件是:物質具有可燃性、與氧氣接觸、達到著火點.
實驗二:鎂條在氧氣中燃燒生成氧化鎂,鎂條在氮氣中能燃燒生成Mg3N2固體,鎂條在二氧化碳氣體中燃燒生成碳和氧化鎂,據此作答.
解答 解:實驗一:根據燃燒的條件可知,將針筒中少量的過氧化氫溶液推入瓶中,燃燒匙的白磷仍沒有燃燒,是因為未達到白磷的著火點;推入H2O2溶液后,生成氧氣,氧氣通過導管進入燒杯,燒杯中的白磷與氧氣接觸,溫度達到了著火點.所以觀察到燒杯中的現象是:導管口有氣泡冒出,導管口處的白磷燃燒;由此可知,可燃物燃燒需要具備的條件是 與氧氣接觸和達到著火點.
實驗二:鎂條在氧氣中燃燒生成氧化鎂,鎂條在氮氣中能燃燒生成Mg3N2固體,鎂條在二氧化碳氣體中燃燒生成碳和氧化鎂,所以引燃燃燒匙中的鎂條,塞還橡皮塞,實驗結束后,觀察到廣口瓶中的現象是進入集氣瓶中水的體積約為其容積的70%,3Mg+N2$\frac{\underline{\;點燃\;}}{\;}$Mg3N2,2Mg+CO2$\frac{\underline{\;點燃\;}}{\;}$C+2MgO,由此可知:鎂條在空氣中燃燒消耗的不只有氧氣,所以不能利用鎂條燃燒來測定空氣中氧氣的體積分數.
故答為:
實驗一:未達到白磷的著火點;導管口有氣泡冒出,導管口處的白磷燃燒;與氧氣接觸;達到著火點.
實驗二:進入集氣瓶中水的體積約為其容積的70%;3Mg+N2$\frac{\underline{\;點燃\;}}{\;}$Mg3N2;2Mg+CO2$\frac{\underline{\;點燃\;}}{\;}$C+2MgO;不能.
點評 此題考查燃燒的條件、化學方程式的書寫、壓強的變化等知識及實驗室探究空氣成分不選擇鎂做燃料的道理,有一定的難度.


 名校課堂系列答案
名校課堂系列答案科目:初中化學 來源: 題型:實驗探究題
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題

查看答案和解析>>
科目:初中化學 來源: 題型:計算題
| 第1次 | 第2次 | 第3次 | 第4次 | 第5次 | 第6次 | |
| 加入稀硫酸的質量(g) | 10 | 10 | 10 | 10 | 10 | 10 |
| 剩余固體的質量(g) | 9.35 | m | 8.05 | 7.4 | 6.75 | 6.75 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com