
4.C
3.D (“防患于未然”與后面語義重復。 “不折不扣”,表示完全的、十足的,在A句中修飾“流水線”,使用正確。“氣勢磅礴”是形容人或事物表現出的力量,氣勢雄偉、盛大,用在B句,符合語境。“恨鐵不成鋼”意為“恨某人不爭氣、不成材。多用于對學生或子女,有時也用于對下屬或公眾人物”,C句中是把《新劇本》當作師長來看的,因而“恨鐵不成鋼”使用正確。)
2.A.( ① 放達:言行不受世俗禮法的拘束;曠達:心胸開闊,想得開。② 互動:共同參與,互相推動;互補:互相補充,此意已包含在前面“互涵”之中了。③ 吞噬:吞吃掉,比喻奪取生命;吞蝕:侵吞,侵蝕。 ④ 根據前后語意,前空用轉折“但”,強調轉折后的語意;后空用“才”,因為兩句之間隱含著必要條件關系,而非充分條件關系。)
1.C.(A.踽踽jǔjǔ B.伺sì 戳-戮 D.紋-文 根-跟)
一個七月的黃昏 ① 一抹淡淡的憂傷
暮色鍍亮彎彎的荷塘 ② 黃昏的衣裳
溫婉的女子依窗 ③ 從指間劃過的是
低低吟唱 ④ 一抹淡淡的殘陽
西閣樓上慵懶的書卷 和 ⑤ 時光的淚痕呀 沾濕了
一抹淡淡的殘陽 ⑥ 從指間劃過
A.④②⑥③⑤① B.⑥③④⑤②① C.④⑥③①⑤② D.⑥③①⑤②④
5.下列各句中,沒有語病的一項是( )
A.著名清代詩人袁枚來岳麓山游賞,據唐人杜牧《山行》中“停車坐愛楓林晚,霜葉紅于二月花”的詩句,將“愛楓亭”之名改成了“愛晚亭”。
B.新的環境倫理則在更理性的層面上告訴人們,鄉土野草是值得尊重和愛惜的,它們對于人類和非人類的價值絕不亞于紅皮書上的一類或二類保護植物。
C.今年9月10日起,又一批方便民眾、還政于民特色的行政法規開始實施,得到了眾多媒體的一致好評。
D.開篇就寫憂國憂民者,敢稱自己是“中國的托爾斯泰”;下筆愛寫個現代詩的,則欣然以“東方泰戈爾”自居:這些初出茅廬的青年作者可真是大言不慚啊!
3.常見配平方法
(1)化合價升降法(即電子得失法或氧化數法)
這類方法既可以配平分子反應式,也可以配平離子反應式,它是氧化還原反應的一般配平方法。化合價升降法的配平步驟是:
①寫出反應物和生成物的化學式,分別標出變價元素的化合價,得出升降數目。
②使化合價升高與化合價降低的總數相等(求最小公倍數法)。
③用觀察的方法配平其它物質的化學計算數(包括部分未被氧化或還原的原子(原子團)數通過觀察法增加到有關還原劑或氧化劑的化學計量數上),配平后把單線改成等號。
該基本步驟可簡記作:劃好價、列變化、求總數、配化學計量數。
例3.由硫可制得多硫化鈉Na2Sx,x值一般為2-6,已知Na2Sx與NaClO反應的化學方程式如下:
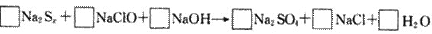
試配平上述方程式,若某多硫化鈉在反應中消耗的NaClO和NaOH的物質的量之比為2:1,試以求得的x值寫出該多硫化鈉的分子式_____________。
解析:本題解答的關鍵必須正確標出Na2Sx中硫的氧化數(化合價),由化合物中化合價的代數和等于零這一原則得硫的氧化數為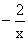 。分析反應前后元素的化合價變化情況,硫元素由
。分析反應前后元素的化合價變化情況,硫元素由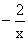 升高到十6價,每個硫原子凈升高數為
升高到十6價,每個硫原子凈升高數為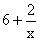 ,x個硫原子共升高6x十2,NaClO中氯元素的化合價由十1價降到-1價,凈降低數為2,根據最小公倍數可得Na2Sx前的系數為1,NaClO和NaCl前的系數為3x十1。
,x個硫原子共升高6x十2,NaClO中氯元素的化合價由十1價降到-1價,凈降低數為2,根據最小公倍數可得Na2Sx前的系數為1,NaClO和NaCl前的系數為3x十1。 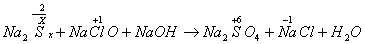 其他物質前面的系數使用觀察法配平。根據NaClO和NaOH的物質的量之比為2:1有:(3x十1)/(2x-2)=2,算出x=5。
其他物質前面的系數使用觀察法配平。根據NaClO和NaOH的物質的量之比為2:1有:(3x十1)/(2x-2)=2,算出x=5。
答案: 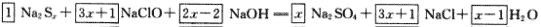 多硫化鈉的化學式為Na2S5。
多硫化鈉的化學式為Na2S5。
例4. 在氯氧化法處理含CN-的廢水過程中,液氯在堿性條件下可以將氰化物氧化成氰酸鹽(其毒性僅為氰化物的千分之一),氰酸鹽進一步被氧化為無毒物質。
(1)某廠廢水中含KCN,其濃度為650mg·L-1現用氯氧化法處理,發現如下反應(其中N均為-3價):KCN+2KOH+Cl2=KOCN+2KCl+H2O被氧化的元素是_________。
(2)投入過量液氯,可將氰酸鹽進一步氧化為氮氣,請配平下列化學方程式,并標出電子轉移方向和數目:
KOCN+ KOH+Cl2 →C02+ N2+______KCl+ ______ H2O
解析: (1)在反應KCN+2KOH+C12→KOCN+2KCl+ H20中,碳元素的化合價從+2上升到+4,失電子被氧化。 (2)從:KCN+KOH+C12→CO2+N2+KCl+ H20可知,N、C兩元素的化合價從-3、-2分別升至0、+4,而C1元素的化合價從0降至-1,根據氧化還原反應中元素化合價升降數相等的規律,即可配得2KCN+4KOH+3C12→2C02+N2 +6KCl+2H20
答案:(1)碳(或C);(2)2;4、3、2、1、6、2
(2)離子-電子法(半反應法)
此方法是將反應式改寫為氧化和還原兩個半反應,先將半反應配平,然后將這些半反應加合起來,消去其中的電子,便完成了配平.此類方法比較適用于某些化合物中元素的氧化數比較難于確定的反應方程式,適用于溶液中的氧化還原反應的配平。
例5.配平MnO4-+ C3H7OH→Mn2++C2H5COOH(酸性介質)
解析:任何一個氧化還原反應都是由兩個半反應組成的。因此可以將這個方程式分成兩個未配平的半反應式,一個代表氧化,一個代表還原。對于此反應可以寫成:
MnO4-→Mn2+(還原) C3H7OH→C2H5COOH(氧化)。由于反應在酸性介質中進行,加H+和H2O配平半反應式兩端的氫原子數,并使兩端電荷數相等:
MnO4-+8H++5e--=Mn2++4H2O①
C3H7OH+H2O= C2H5COOH+4H++4e-②
根據得失電子數必須相等,將兩邊電子消去,加合成一個已配平的反應式。
①×4+②×5得:4MnO4-+12H++5C3H7OH =4Mn2++5C2H5COOH+11H2O
經檢驗:配平正確。
(3)自身氧化還原反應方程式的逆向配平法
自身氧化--還原反應是電子轉移發生于同一種物質的同一種元素間或同一種物質分子內部不同種元素間的氧化--還原反應。從化學反應方程式的生成物一側入手,從右向左進行配平。
例如:配平Cl2+KOH--KCl+KClO3+H2O
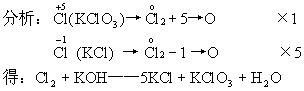
KCl和KClO3系數之和除2,就是Cl2的系數,其余系數再通過觀察確定。
即:3Cl2+6KOH  5KCl+KClO3+3H2O
5KCl+KClO3+3H2O
說明:在化合價升降法的基礎上采用逆向配平的方法。有助于培養辯證思維,是對傳統方法的創新。
2.配平的思路
一般分兩部分:第一部分是氧化劑、還原劑、氧化產物、還原產物之間的配平-化合價升降相等或電子得失數相等;第二部分是用觀察法配平其他物質的化學計量數。
1.配平的原則
(1)電子守恒:氧化還原反應過程中,氧化劑得電子總數目等于還原劑失電子總數目,即:“電子得失數相等”“化合價升降數相等”。
(2)質量守恒:反應前后各元素的原子個數相等。
(3)電荷守恒:對于離子方程式,等式兩邊“電荷總數相等”。
原理是:氧化劑得到的電子總數等于還原劑失去的電子總數。
例2.硫酸銨在強熱條件下分解,生成氨、二氧化硫、氮氣和水.反應中生成的氧化產物和還原產物的物質的量之比是( )
A.1:3 B.2:3 C.1:1 D.4:3
解析:首先判斷氧化產物是氮氣,還原產物是二氧化硫。每生成1摩爾氮氣需要失去6摩爾電子,每生成1摩爾二氧化硫需要得到2摩爾電子。根據得失電子相等的原理,氧化產物和還原產物的物質的之比應為1:3。
答案:A
說明:解這類題目不必都寫出完整并配平的氧化還原反應方程式,關鍵是抓住本質,厘清得失相等的關系。
2.常用判斷方法
(1)依據元素在同期表的位置判斷
從左到右:金屬單質的還原性依次減弱,非金屬單質的氧化性逐漸加強。
從上到下:金屬單質的還原性依次增強,非金屬單質的氧化性逐漸減弱。
單質氧化性:F2>Cl2>Br2>I2>S
離子還原性:S2_>I->Br->Cl->F-
單質還原性:Na>Mg>Al
離子氧化性:Al3+>Mg2+>Na+
(2)根據金屬的活動性順序表來判斷

(3)通過氧化還原反應比較:氧化劑+還原劑 氧化產物+還原產物
氧化產物+還原產物
氧化性:氧化劑>氧化產物 還原性:還原劑>還原產物
(4)通過與同一物質反應的產物比較:如:2Fe+3Cl2 ======2FeCl3 ,Fe+S======FeS ,可得出氧化性Cl2 >S。
(5)反應原理相似的不同反應中,反應條件要求越低,說明氧化劑或還原劑越強。
如鹵素單質與H2的反應,按F2、Cl2、Br2、I2的順序反應越來越難,反應條件要求越來越高,則可得出氧化性F2>Cl2 >Br2 >I2 。
(6)對同一元素而言,一般價態越高,氧化性越強,如Fe3+>Fe2+>Fe;價態越低,氧化性越弱,如S2―<S<SO2。(特例:氧化性HClO>HClO2>HClO3>HClO4 )
(7)據原電池電極:負極金屬比正極金屬活潑(還原性強);據電解池中放電順序,先得(或失)電子者氧化性(或還原性)強,其規律為:陽離子得電子順序(即氧化性強弱順序):參考②中規律。陰離子失電子順序(即還原性強弱順序):S2->I->Br->Cl->OH->NO3- 、SO42-等。
說明:氧化性與還原性受外界因素的影響。
溫度:溫度高時,氧化劑的氧化性和還原劑的還原性均增強。如濃H2SO4具有強氧化性,熱的濃H2SO4比冷的濃H2SO4氧化性要強。
濃度:濃度大時,氧化劑的氧化性和還原劑的還原性均增強。如濃H2SO4具有強氧化性,稀硫酸只有H+顯示弱氧化性。
酸堿性:如KMnO4的氧化性隨溶液酸性的增強而增強。在酸性環境中,KMnO4的還原產物為Mn2+;在中性環境中,KMnO4的還原產物為MnO2;在堿性環境中,KMnO4的還原產物為K2MnO4 。在使用高錳酸鉀作為氧化劑檢驗或除雜一些還原性物質時,為了現象明顯,反應快速。往往使用酸性高錳酸鉀溶液。
例1.常溫下,在下列溶液中發生如下反應: ①16H+十10Z-十2XO4-=2x2+十5Z2十8H2O ②2A2++B2=2A3+十2B- ③2B-十Z2=B2十2Z- 由此判斷下列說法錯誤的是( ) A.反應Z2十2A2+=2A3+十2Z-可以進行 B.Z元素在①③反應中均被還原 C.氧化性由強到弱的順序是XO4-、Z2、B2、A3+
D.還原性由強到弱的順序是A2+、B-、Z-、X2+ 解析:根據規律,在同一反應中,氧化劑的氧化性大于氧化產物的氧化性,還原劑的還原性大于還原產物的還原性,得出:氧化性XO4->Z2>B2>A3+,還原性A2+>B->Z->X2+。
答案:B
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com