
科目: 來源: 題型:
【題目】恒溫、恒壓下,1 mol A和1 mol B在一個容積可變的容器中發生如下反應:A(g)+2B(g) ![]() 2C(g)。一段時間后達到平衡,生成a mol C。下列說法不正確的是
2C(g)。一段時間后達到平衡,生成a mol C。下列說法不正確的是
A. 起始時刻和達到平衡后容器中的壓強比為1:1
B. 物質A、B的轉化率之比一定是1:2
C. 若起始放入3 mol A和3 mol B,則達到平衡時生成3a mol C
D. 當v正(A)=v逆(B)時,可斷定反應達到平衡
查看答案和解析>>
科目: 來源: 題型:
【題目】“磷酸氯喹”是抗擊新型冠狀病毒的潛在藥物,其合成路線如下:
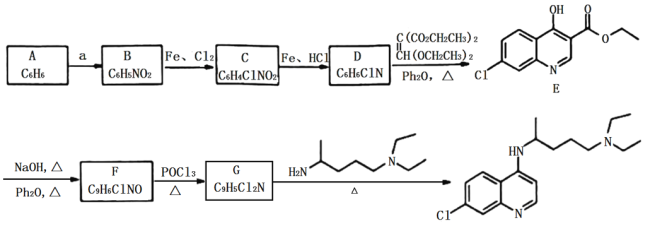
已知: 
![]()

(1)A是一種芳香烴,試劑a為:____________________。
(2)B反應生成C的反應化學方程式為____________________。
(3)由C生產D和由F生成G的反應類型分別為__________、___________。
(4)D的結構簡式為_________。
(5)E中含氧官能團的名稱為________。
(6)I與E互為同分異構體,且具有完全相同的官能團,符合下列條件的I有____種。(不考慮立體異構)
①分子結構中含有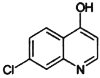 ;②分子中環狀結構上只有三個取代基。寫出其中任意兩種結構簡式____、______。
;②分子中環狀結構上只有三個取代基。寫出其中任意兩種結構簡式____、______。
(7)有機物J(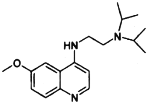 )是治療血吸蟲病的藥物,參照上述
)是治療血吸蟲病的藥物,參照上述![]() 的合成路線,設計由4-甲氧基苯氨(
的合成路線,設計由4-甲氧基苯氨( )和N,N-二異丙基乙二胺(
)和N,N-二異丙基乙二胺(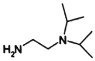 )為起始原料制備有機J的合成路線_______________________(無機試劑任意選用)。
)為起始原料制備有機J的合成路線_______________________(無機試劑任意選用)。
查看答案和解析>>
科目: 來源: 題型:
【題目】某燒堿樣品含有少量不與酸作用的雜質,為了測定其純度,進行以下滴定操作:
A. 在250 mL的容量瓶中定容配制250 mL燒堿溶液;
B. 用堿式滴定管移取25.00 mL燒堿溶液于錐形瓶中并滴入2滴甲基橙指示劑;
C. 在天平上準確稱取燒堿樣品2.0 g,在燒杯中用蒸餾水溶解;
D. 將物質的量濃度為0.100 0 mol·L-1的標準鹽酸裝入酸式滴定管,調整液面記下開始讀數為V1;
E. 在錐形瓶下墊一張白紙,滴定至終點,記下讀數V2。
就此實驗完成下列填空:
(1)正確的操作步驟的順序是(用編號字母填寫)
________→________→________→D→________。
(2)上述E中錐形瓶下墊一張白紙的作用是_______________________________
(3)用標準的鹽酸滴定待測的NaOH溶液時,左手握酸式滴定管的活塞,右手搖動錐形瓶,眼睛注視______________。直到加入一滴鹽酸后,溶液____________________________ (填顏色變化)。
(4)下列操作中可能使所測NaOH溶液的濃度數值偏低的是(____________)
A.酸式滴定管未用標準鹽酸潤洗就直接注入標準鹽酸
B.滴定前盛放NaOH溶液的錐形瓶用蒸餾水洗凈后沒有干燥
C.酸式滴定管在滴定前有氣泡,滴定后氣泡消失
D.讀取鹽酸體積時,開始仰視讀數,滴定結束時俯視讀數
(5)若滴定開始和結束時,酸式滴定管中的液面如圖所示,則所用鹽酸溶液的體積為________mL。

(6)某學生根據3次實驗分別記錄有關數據如表:
滴定 次數 | 待測NaOH溶液的體積/mL | 0.100 0 mol·L-1鹽酸的體積/mL | ||
滴定前 刻度 | 滴定后刻度 | 溶液體積/mL | ||
第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
依據上表數據列式計算該燒堿的純度____。(結果保留四位有效數字)
查看答案和解析>>
科目: 來源: 題型:
【題目】醋酸亞鉻水合物[Cr(CH3COO)2]22H2O (相對分子質量為376)是一種氧氣吸收劑,為紅棕色晶體,潮濕時易被氧化,微溶于乙醇,不溶于水和乙醚(易揮發的有機溶劑)。其制備裝置及步驟如下:
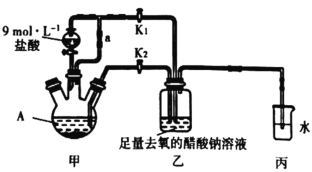
①________________________________________。
②往裝置A中依次加入過量鋅粒、適量CrCl3溶液。
③關閉K2,打開K1,旋開分液漏斗的旋塞并控制好滴速。
④待A內的溶液由深綠色(Cr3+)變為亮藍色(Cr2+)時,將溶液轉移至裝置乙中,當出現大量紅棕色晶體時,關閉分液漏斗的旋塞。
⑤將裝置乙中混合物快速過濾、洗滌和干燥,稱量得到[Cr(CH3COO)2]22H2O。
(1)實驗步驟①進行什么操作______________________________。
(2)裝置A的名稱__________________。
(3)寫出裝置A中反應的離子方程式為__________________,___________________________。
(4)實現步驟①中溶液自動轉移至裝置乙中的實驗操作為__________________。
(5)步驟③目的是_____________________________________________。
(6)洗滌產品時,依次用去氧的冷蒸餾水、無水乙醇、乙醚,目的是__________________。
(7)已知其它反應物足量,實驗時取用的CrCl3溶液中含溶質12.68g,實驗后得干燥純凈的[Cr(CH3COO)2]22H2O 11.28g,則該實驗所得產品的產率為_______(不考慮溶解的醋酸亞鉻水合物)(用百分數表示,保留3位有效數字)。
查看答案和解析>>
科目: 來源: 題型:
【題目】將1molI2和2molH2(g)置于某2L密閉容器中,在—定溫度下發生反應:I2(g)+H2(g)![]() 2HI(g) △H<0,并達平衡,HI的體積分數ω(HI)隨時間變化如圖曲線
2HI(g) △H<0,并達平衡,HI的體積分數ω(HI)隨時間變化如圖曲線

(1)達平衡時,I2(g)的物質的量濃度為 _______。H2(g)的平衡轉化率為___________。
在此溫度下,該反應的平衡常數K__________(保留一位小數)。
(2)若改變反應條件下,在甲條件下ω(HI)的變化如圖曲線(I)所示,在乙條件下ω(HI)的變化如圖曲線(III)所示。則甲條件可能是______(填入下列條件的序號。下同),乙條件可能是________。
①恒容條件下,升高溫度
②恒容條件下,降低溫度
③恒溫條件下,縮小反應容器體積
④恒溫條件下,擴大反應容器體積
⑤恒溫恒容條件下,加入適當催化劑
(3)若保持溫度不變,在另一相同的2L密閉容器中加入a mol I2(g)、b mol H2和c mol HI(a、b、 c均大于0),發生反應,達平衡時,HI的體積分數仍為0.60,則a、b、c的應滿足的關系是_______________ (用含一個a、b、c的代數式表示)
查看答案和解析>>
科目: 來源: 題型:
【題目】![]() 、
、![]() 、
、![]() 、
、![]() 、S、P等元素常用于化工材料的合成。回答下列問題:
、S、P等元素常用于化工材料的合成。回答下列問題:
(1)鈷原子的基態電子排布式為_______________________。
(2)![]() 有________幾種不同的運動狀態的電子,
有________幾種不同的運動狀態的電子,![]() 比
比![]() 更穩定的原因是_________。
更穩定的原因是_________。
(3)硒為第四周期元素,相鄰元素有砷和溴,則三種元素的電負性從大到小的順序為_________(用元素符號表示)。
(4)![]() 的熔點為340℃,加熱易升華,固體
的熔點為340℃,加熱易升華,固體![]() 屬于______晶體。
屬于______晶體。![]() 的空間構型為_____。
的空間構型為_____。
(5) ![]() 可用于制造火柴,其分子結構如圖甲所示。
可用于制造火柴,其分子結構如圖甲所示。![]() 分子中S的雜化方式為______。每個
分子中S的雜化方式為______。每個![]() 分子中含有的孤電子對的數目為_________。
分子中含有的孤電子對的數目為_________。


(6)銅的某種氧化物晶胞結構如圖乙所示,該氧化物的化學式為____________。若該晶胞的邊長為![]() ,阿伏加德羅常數值為
,阿伏加德羅常數值為![]() ,則該氧化物的密度為_________
,則該氧化物的密度為_________![]()
查看答案和解析>>
科目: 來源: 題型:
【題目】含碳化合物在生產生活中廣泛存在。請回答下列問題:
(1)Andren Dasic等提出在金屬催化劑M的作用下以![]() 為氧化劑可以氧化乙烯生成乙醛,催化體系氧化還原循環如圖1所示。(物質與氧原子的結合力用
為氧化劑可以氧化乙烯生成乙醛,催化體系氧化還原循環如圖1所示。(物質與氧原子的結合力用![]() 表示),氧原子與
表示),氧原子與![]() 生成
生成![]() 的結合力
的結合力![]() ,氧原子與乙烯生成乙醛的結合力
,氧原子與乙烯生成乙醛的結合力![]() ,則可做該反應催化劑的金屬M與氧原子的結合力
,則可做該反應催化劑的金屬M與氧原子的結合力![]() (M)的值應滿足_______。使用催化劑會使該反應的活化能______(填“增大”、“減小”、“不變”)。
(M)的值應滿足_______。使用催化劑會使該反應的活化能______(填“增大”、“減小”、“不變”)。

(2)已知![]() 、
、![]() 、
、![]() 的燃燒熱分別為
的燃燒熱分別為![]() 、
、![]() 、
、![]() 。
。
則反應:![]() ΔH=_________。
ΔH=_________。
(3)已知在含少量的![]() 溶液中,反應
溶液中,反應![]() 分兩步進行:第Ⅰ步反應
分兩步進行:第Ⅰ步反應![]() (慢反應),第Ⅱ步為快反應。
(慢反應),第Ⅱ步為快反應。
①請寫出第二步反應的化學方程式:____________。
②增大濃度![]() 濃度______(填“能”或“不能”)明顯增大總反應的平均速率,理由為__________。
濃度______(填“能”或“不能”)明顯增大總反應的平均速率,理由為__________。
(4)某密閉容器中發生:![]() ,
,![]() 在不同溫度下平衡分解的情況如圖2所示。
在不同溫度下平衡分解的情況如圖2所示。


①圖中a、b、c三點的平衡常數![]() 的大小關系為_____________。
的大小關系為_____________。
②恒溫恒容條件下,能表示該可逆反應達到平衡狀態的是____________(填標號)
A.![]() 體積分數與
體積分數與![]() 體積分數的比值保持不變
體積分數的比值保持不變
B.容器內混合氣體的密度保持不變
C.容器內混合氣體的平均摩爾質量保持不變
D.容器內碳元素的質量分數保持不變
③為實現![]() 減排,目前較成熟的方法是用高濃度的
減排,目前較成熟的方法是用高濃度的![]() 溶液吸收工業煙氣中的
溶液吸收工業煙氣中的![]() ,得溶液X,再利用電解法使
,得溶液X,再利用電解法使![]() 溶液再生,其裝置示意圖如圖3,簡述
溶液再生,其裝置示意圖如圖3,簡述![]() 在陰極區再生的原理_______。
在陰極區再生的原理_______。
查看答案和解析>>
科目: 來源: 題型:
【題目】將鎂鋁鐵合金投入到300 mL硝酸溶液中,金屬恰好完全溶解生成Mg2+、Al3+和Fe3+;硝酸全部被還原為一氧化氮,其體積為6.72 L(標準狀況),當加入300 mL某濃度氫氧化鈉溶液時,金屬陽離子恰好全部沉淀,干燥后測得質量為27.2 g。下列有關推斷正確的是( )
A. 參加反應的硝酸的物質的量為0.9 mol
B. 參加反應的金屬的質量為11.9 g
C. 硝酸的物質的量濃度為3 mol·L-1
D. 氫氧化鈉的物質的量濃度為6 mol·L-1
查看答案和解析>>
科目: 來源: 題型:
【題目】下列有關氨的敘述中不正確的是( )
A. 氨分子中氮元素的化合價只能升高,氨具有還原性
B. 氨的催化氧化反應的化學方程式是4NH3+5O2![]() 4NO+6H2O
4NO+6H2O
C. 氨的催化氧化反應中若氧氣過量則有紅棕色氣體生成
D. 氨的催化氧化屬于人工氮的固定
查看答案和解析>>
科目: 來源: 題型:
【題目】 對于平衡體系:mA(g)+ nB(g)![]() pC(g)+ qD(g),下列判斷正確的是( )
pC(g)+ qD(g),下列判斷正確的是( )
A.若溫度不變將容器的容積增大1倍,達到新平衡時A的濃度變為原來的0.45 倍,則m+n>p+q
B.若平衡時,A、B的轉化率相等,說明反應開始時,A、B的物質的量之比為m:n
C.若升高平衡體系的溫度,達到新平衡時A 的濃度變為原來的0.55 倍,說明該反應△ H<0
D.若平衡后同時增大A、B的濃度,則A、B的轉化率一定都減小
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com