
【題目】下列有關氨的敘述中不正確的是( )
A. 氨分子中氮元素的化合價只能升高,氨具有還原性
B. 氨的催化氧化反應的化學方程式是4NH3+5O2![]() 4NO+6H2O
4NO+6H2O
C. 氨的催化氧化反應中若氧氣過量則有紅棕色氣體生成
D. 氨的催化氧化屬于人工氮的固定
【答案】D
【解析】
A、氮元素的常見化合價有-3、0、+2、+4、+5價,氨氣分子中氮元素是-3價,為最低價態;
B、氨氣具有還原性,在催化劑作用下可與氧氣反應被氧化為NO;
C、若氧氣過量,生成的一氧化氮氣體與氧氣反應生成紅棕色氣體二氧化氮;
D、氨的催化氧化是氮的化合態之間的轉化,不屬于氮的固定。
A項、氨氣分子中氮元素是-3價,是氮元素的最低價態,所以只具有還原性,故A正確;
B項、氨氣具有還原性,在催化劑作用下可與氧氣反應被氧化為NO,反應的化學方程式是4NH3+5O2![]() 4NO+6H2O,故B正確;
4NO+6H2O,故B正確;
C項、氨催化氧化反應是氨氣在催化劑作用下被氧氣氧化為一氧化氮的反應,若氧氣過量,生成的一氧化氮氣體與氧氣反應生成紅棕色氣體二氧化氮,故C正確;
D項、NH3催化氧化生成NO和H2O,是氮的化合態之間的轉化,不屬于氮的固定,故D錯誤。
故選D。


 紅果子三級測試卷系列答案
紅果子三級測試卷系列答案 課堂練加測系列答案
課堂練加測系列答案科目:高中化學 來源: 題型:
【題目】下列關于膠體的敘述中,不正確的是( )
A.![]() 膠體能吸附水中的懸浮顆粒并沉降,常用于凈水
膠體能吸附水中的懸浮顆粒并沉降,常用于凈水
B.濁液、膠體、溶液的本質區別是分散質粒子的直徑大小
C.用激光筆照射![]() 溶液和
溶液和![]() 膠體時,產生的現象相同
膠體時,產生的現象相同
D.膠態磁流體治癌術是將磁性物質制成膠體粒子,這種粒子的直徑在![]() 之間
之間![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】25℃、101 kPa時,1 g甲醇(CH3OH)完全燃燒生成CO2和液態H2O,同時放出22.68 kJ熱量。下列表示該反應的熱化學方程式中正確的是( )
A.CH3OH(l)+![]() O2(g)=CO2(g)+2H2O(l) ΔH=-725.8 kJ/mol
O2(g)=CO2(g)+2H2O(l) ΔH=-725.8 kJ/mol
B.2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ΔH=+1 451.6 kJ/mol
C.2CH3OH+3O2=2CO2+4H2O(l) ΔH=-22.68 kJ/mol
D.CH3OH(l)+![]() O2(g)=CO2(g)+2H2O(g) ΔH=-725.8 kJ/mol
O2(g)=CO2(g)+2H2O(g) ΔH=-725.8 kJ/mol
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下面是石蠟油在熾熱碎瓷片的作用下產生乙烯并檢驗乙烯性質的實驗,請回答下列問題:

(1)A中碎瓷片的作用是________。
(2)B裝置中反應的化學方程式為__________。
(3)C裝置中可觀察到的現象是_________。
(4)查閱資料.乙烯與酸性高錳酸鉀溶液反應產生二氧化碳,根據本實驗中裝置_____(填裝置字母)中的實驗現象可判斷該資料是否直實。
(5)通過上述實驗探究,檢驗甲烷和乙烯的方法是_______(填字母,下同),除去甲烷中乙烯的方法是___。
A 氣體通入水中 B 氣體通過盛溴水的洗氣瓶
C 氣體通過盛酸性高錳酸鉀溶液的洗氣瓶 D 氣體通過氫氧化鈉溶液
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將4 mol A氣體和2 mol B氣體在2 L的定容密閉容器中混合,并在一定條件下發生如下反應:2A(g)+B(g)![]() 2C(g);經2 s后測得C的物質的量濃度為0.6 mol·L-1,現有下列幾種說法:
2C(g);經2 s后測得C的物質的量濃度為0.6 mol·L-1,現有下列幾種說法:
①用物質A表示的這段時間的平均速率為0.3 mol·L-1·s-1
②用物質B表示的這段時間的平均速率為0.6 mol·L-1·s-1
③2 s時物質A的轉化率為30%
④2 s時物質B的物質的量濃度為0.3 mol·L-1
其中正確的是
A. ①③ B. ②④ C. ①② D. ③④
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知亞硫酸鈉晶體與濃硫酸反應可以產生二氧化硫,按下圖進行演示實驗。
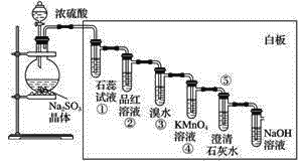
請回答下列問題:
(1)①中的實驗現象是__________,說明二氧化硫具有的性質是__________。
(2)②中的實驗現象是__________,證明二氧化硫有___________性。
(3)③中的實驗現象是_______________,證明二氧化硫有____________性。
(4)④中的實驗現象是__________,證明二氧化硫有______性。
(5)⑤中的實驗現象是_____________,說明二氧化硫具有的性質是_____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】我國是世界上較早冶煉鋅的國家。在現代工業中,鋅更是在電池制造、合金生產等領域有著廣泛的用途。
已知:鋅的熔點為419.6℃,沸點907℃。
I.圖是古代以爐甘石(ZnCO3)為原料煉鋅的示意圖。
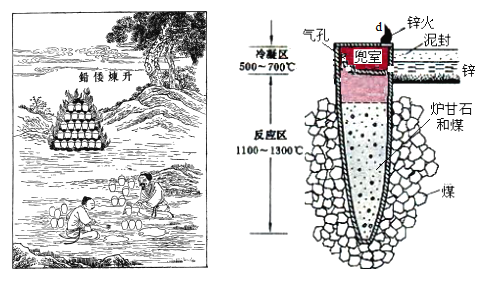
(1)泥罐內的主要反應為:
i.ZnCO3(s) = ZnO(s) + CO2(g) H1
ii.CO2(g) + C(s) = 2CO(g) H 2
……
總反應:ZnCO3(s) + 2C(s) = Zn(g) + 3CO(g) H3
利用H1和H 2計算時H3,還需要利用_________反應的H。
(2)泥罐中,金屬鋅的狀態變化是_____;d口出去的物質主要是_______。
Ⅱ.現代冶煉鋅主要采取濕法工藝。以閃鋅礦(主要成分為ZnS,還含鐵等元素)、軟錳礦(主要成分為MnO2,還含鐵等元素)為原料聯合生產鋅和高純度二氧化錳的一種工藝的主要流程如下:
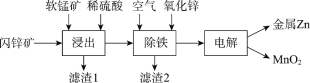
(3)浸出:加入FeSO4能促進ZnS的溶解,提高鋅的浸出率,同時生成硫單質。Fe2+的作用類似催化劑,“催化”過程可表示為:
ⅰ:MnO2+2Fe2++4H+ =Mn2++2Fe3++2H2O
ⅱ:……
① 寫出ⅱ的離子方程式:_________。
② 下列實驗方案可證實上述“催化”過程。將實驗方案補充完整。
a.向酸化的FeSO4溶液中加入KSCN溶液,溶液幾乎無色,再加入少量MnO2,溶液變紅。
b.________。
(4)除鐵:已知①進入除鐵工藝的溶液的pH約為3;②控制溶液pH為2.5~3.5,使鐵主要以FeOOH沉淀的形式除去。結合離子方程式說明,通入空氣需同時補充適量ZnO的理由是_________。
(5)電解:用惰性電極電解時,陽極的電極反應是______。
(6)電解后的溶液中可循環利用的物質是___________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業生產硫酸中二氧化硫的催化氧化原理為:2SO2(g)+O2(g)![]() 2SO3(g),反應混合體系在平衡狀態時SO3的百分含量與溫度的關系如下圖所示。下列說法錯誤的是
2SO3(g),反應混合體系在平衡狀態時SO3的百分含量與溫度的關系如下圖所示。下列說法錯誤的是

A. 在A、B、C三點時,V(正)=v(逆),在D點時V(正)>v(逆)
B. A、B、C三點的平衡常數一定不相同
C. 升高溫度可以加快化學反應速率,有利于平衡向正反應方向移動
D. 一定溫度下,保持容器體積不變,向平衡體系中通人稀有氣體,壓強增大,平衡不移動
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】科研人員利用Cu/ZnO作催化劑,在光照條件下實現了CO2和H2合成CH3OH,該反應歷程示意圖如下。
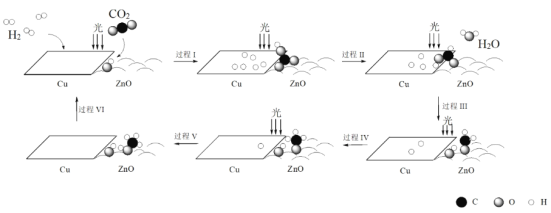
下列說法不正確的是
A.過程I中ZnO表面上進行CO2的吸附與轉化
B.過程II中存在極性鍵的斷裂與形成
C.過程V中生成CH3OH時吸收能量
D.總反應的化學方程式是CO2 + 3H2![]() CH3OH + H2O
CH3OH + H2O
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com