
科目: 來源:2016-2017學年四川省高二下學期開學考試化學試卷(解析版) 題型:選擇題
將4mol A氣體和2mol B氣體在2L的容器中混合并在一定條件下發生如下反應:2A(g)+B(g)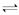 2C(g)。若經2s后測得C的濃度為0.6mol/L,現有幾種說法:
2C(g)。若經2s后測得C的濃度為0.6mol/L,現有幾種說法:
①用物質A表示的反應的平均速率為0.3 mol/(L·s)
②用物質B表示的反應的平均速率為0.6 mol/(L·s )
③2s時物質A的轉化率為70% ④2s時B物質的濃度為0.7 mol/L
其中正確的是( )
A. ①③ B. ①④ C. ②③ D. ③④
查看答案和解析>>
科目: 來源:2016-2017學年四川省高二下學期開學考試化學試卷(解析版) 題型:選擇題
某密閉容器中充入等物質的量的氣體A和B,一定溫度下發生反應A(g)+xB(g)  2C(g),達到平衡后,只改變反應的一個條件,測得容器中各物質的濃度、反應速率隨時間變化的關系如圖所示。下列說法正確的是( )
2C(g),達到平衡后,只改變反應的一個條件,測得容器中各物質的濃度、反應速率隨時間變化的關系如圖所示。下列說法正確的是( )
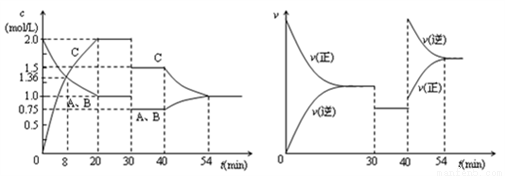
A. 前20min B的平均反應速率為0.05mol·L-1·min-1
B. 8 min時表示正反應速率等于逆反應速率
C. 反應方程式中的x=1,30 min時表示增大壓強
D. 40 min時改變的條件是升高溫度,且正反應為吸熱反應
查看答案和解析>>
科目: 來源:2016-2017學年四川省高二下學期開學考試化學試卷(解析版) 題型:選擇題
下列有關晶體的敘述中,不正確的是
A. 氯化鈉和氯化銫晶體中,陽離子的配位數均為6
B. 金剛石為立體網狀結構,由碳原子以sp3雜化軌道形成共價鍵
C. 金屬鈉的晶體采用體心立方堆積,每個晶胞含2個原子,配位數為8
D. 干冰晶體中,每個CO2分子周圍緊鄰12個CO2分子
查看答案和解析>>
科目: 來源:2016-2017學年四川省高二下學期開學考試化學試卷(解析版) 題型:選擇題
100℃時,將0.1mol N2O4置于1L密閉的燒瓶中,然后將燒瓶放入100℃的恒溫槽中,燒瓶內的氣體逐漸變為紅棕色:N2O4(g) 2NO2 (g),下列結論不能說明上述反應在該條件下已經達到平衡狀態的是( )
2NO2 (g),下列結論不能說明上述反應在該條件下已經達到平衡狀態的是( )
①N2O4的消耗速率與NO2的生成速率之比為1:2
②NO2生成速率與NO2消耗速率相等
③燒瓶內氣體的壓強不再變化
④燒瓶內氣體的質量不再變化
⑤NO2的物質的量濃度不再改變
⑥燒瓶內氣體的顏色不再加深
⑦燒瓶內氣體的平均相對分子質量不再變化
⑧燒瓶內氣體的密度不再變化
A. ②③⑥⑦ B. ①④⑧ C. 只有①④ D. 只有⑦⑧
查看答案和解析>>
科目: 來源:2016-2017學年四川省高二下學期開學考試化學試卷(解析版) 題型:選擇題
對于密閉容器中可逆反應 A2(g)+3B2(g) 2AB3(g),探究單一條件改變情況下,可能引起平衡狀態的改變,得到如下圖所示的曲線(圖中T表示溫度,n 表示物質的量)下列判斷正確的是
2AB3(g),探究單一條件改變情況下,可能引起平衡狀態的改變,得到如下圖所示的曲線(圖中T表示溫度,n 表示物質的量)下列判斷正確的是
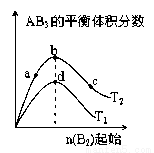
A. 加入催化劑可以使狀態 d 變為狀態 b
B. 若 T1>T2,則逆反應一定是放熱反應
C. 達到平衡時 A2 的轉化率大小為: b>a>c
D. 在T2 和n(A2)不變時達到平衡,AB3 的物質的量大小為: c>b>a
查看答案和解析>>
科目: 來源:2016-2017學年四川省高二下學期開學考試化學試卷(解析版) 題型:實驗題
某實驗小組用0.50 mol/L NaOH溶液和0.50 mol/L硫酸溶液進行中和熱的測定。
Ⅰ.配制0.50 mol/L NaOH溶液
若實驗中大約要使用245 mL NaOH溶液,至少需要稱量NaOH固體_____g。
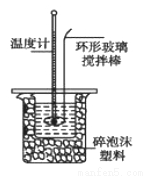
Ⅱ.測定稀硫酸和稀氫氧化鈉中和熱的實驗裝置如圖所示。
(1)寫出該反應的熱化學方程式(中和熱為57.3 kJ/mol):_____________。
(2)取50 mL NaOH溶液和30 mL硫酸溶液進行實驗,實驗數據如下表。
①請填寫下表中的空白:
起始溫度t1/℃ | 終止溫度 t2/℃ | 溫度差平均值 (t2-t1)/℃ | |||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 30.1 | ______ |
2 | 27.0 | 27.4 | 27.2 | 33.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.8 | |
4 | 26.4 | 26.2 | 26.3 | 30.4 | |
②近似認為0.50 mol/L NaOH溶液和0.50 mol/L硫酸溶液的密度都是1 g/cm3,中和后生成溶液的比熱容c=4.18 J/(g·℃)。則中和熱△H=______________取小數點后一位)。
③上述實驗數值結果與57.3 kJ/mol有偏差,產生偏差的原因可能是:______。
A.實驗裝置保溫、隔熱效果差
B.量取NaOH溶液的體積時仰視讀數
C.分多次把NaOH溶液倒入盛有硫酸的小燒杯中
D.用溫度計測定NaOH溶液起始溫度后直接測定H2SO4溶液的溫度
查看答案和解析>>
科目: 來源:2016-2017學年四川省高二下學期開學考試化學試卷(解析版) 題型:簡答題
(一)霧霾天氣肆虐給人類健康帶來了嚴重影響.燃煤和汽車尾氣是造成空氣污染的原因之一.
(1)汽車尾氣凈化的主要原理為:2NO(g)+2CO 2CO2(g)+N2(g)△H<O
2CO2(g)+N2(g)△H<O
①反應的速率-時間圖像如圖甲所示.若其他條件不變,僅在反應前加入合適的催化劑,其速率時間圖象如圖乙所示.以下說法正確的是___________(填對應字母).

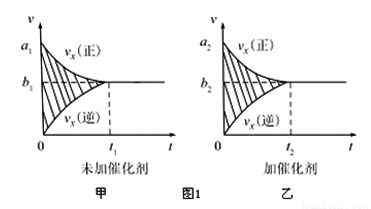
A.a1>a2 B.b1<b2 C.t1>t2
D.圖乙中陰影部分面積更大 E.圖甲中陰影部分面積更大
②若該反應在絕熱、恒容的密閉體系中進行,下列示意圖正確且能說明反應在進行到t1時刻達到平衡狀態的是_________(填代號)
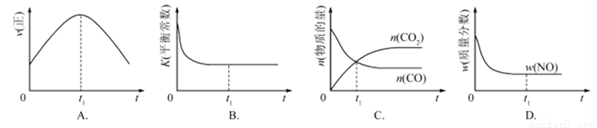
(2)直接排放煤燃燒產生的煙氣會引起嚴重的環境問題.煤燃燒產生的煙氣含氮的氧化物,用CH4催化還原NOx可以消除氮氧化物的污染.
已知:CH4(g)+2NO2(g) N2(g)+CO2(g)+2H2O(g)△H=﹣867kJ/mol
N2(g)+CO2(g)+2H2O(g)△H=﹣867kJ/mol
2NO2(g) N2O4(g)△H=﹣56.9kJ/mol H2O(g)=H2O(l)△H=﹣44.0kJ/mol
N2O4(g)△H=﹣56.9kJ/mol H2O(g)=H2O(l)△H=﹣44.0kJ/mol
寫出CH4催化還原N2O4(g)生成N2和H2O(l)的熱化學方程式:______________.
(3)CH4和H2O(g) 在催化劑表面發生反應CH4+H2O?CO+3H2,該反應在不同溫度下的化學平衡常數如表:
溫度/℃ | 800 | 1000 | 1200 | 1400 |
平衡常數 | 0.45 | 1.92 | 276.5 | 1771.5 |
①該反應是_________反應(填“吸熱”或“放熱”).
②T℃時,向1L密閉容器中投入l mol CH4和l mol H2O(g),平衡時c(CH4)=0.5mol/L,該溫度下反應CH4+H2O CO+3H2的平衡常數K=______________.
CO+3H2的平衡常數K=______________.
(二)恒溫時,將2molA和2molB氣體投入固定容積為2L密閉容器中發生反應:2A(g)+B(g)  xC(g)+D(s),10s時,測得A的物質的量為1.7mol,C的反應速率為0.0225mol·L—1·s—1;40s時反應恰好處于平衡狀態,此時B的轉化率為20%。請填寫下列空白:
xC(g)+D(s),10s時,測得A的物質的量為1.7mol,C的反應速率為0.0225mol·L—1·s—1;40s時反應恰好處于平衡狀態,此時B的轉化率為20%。請填寫下列空白:
(1)x=____________
(2)從反應開始到10s,B的平均反應速率為____________
(3)從反應開始到40s達平衡狀態,A的平均反應速率為____________
(4)平衡時容器中B的體積分數為____________
(5)下列各項能表示該反應達到平衡狀態是____________
A.消耗A的物質的量與生成D的物質的量之比為2∶1
B.容器中A、B的物質的量 n(A)∶n(B) =2∶1
C.氣體的平均相對分子質量不再變化
D.壓強不再變化
E.氣體密度不再變化
查看答案和解析>>
科目: 來源:2016-2017學年四川省高二下學期開學考試化學試卷(解析版) 題型:簡答題
請參考題中圖表,已知E1=134 kJ·mol-1、E2=368 kJ·mol-1,根據要求回答問題:
(1)圖Ⅰ是1 mol NO2(g)和1 mol CO(g)反應生成CO2和NO過程中的能量變化示意圖,若在反應體系中加入催化劑,反應速率增大,E1的變化是__________(填“增大”、“減小”或“不變”,下同),ΔH的變化是__________。請寫出NO2和CO反應的熱化學方程式___________________。

(2)甲醇質子交換膜燃料電池中將甲醇蒸汽轉化為氫氣的兩種反應的熱化學方程式如下:
①CH3OH(g)+H2O(g)==CO2(g)+3H2(g) ΔH=+49.0 kJ·mol-1
②CH3OH(g)+ O2(g)==CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
O2(g)==CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
且H2O(g)==H2O(l) ΔH=-44 kJ·mol-1,則甲醇蒸汽燃燒為液態水的熱化學方程式為_______________。
(3)如表所示是部分化學鍵的鍵能參數:
化學鍵 | P—P | P—O | O===O | P===O |
鍵能/kJ·mol-1 | a | b | c | x |

已知白磷的燃燒熱為d kJ·mol-1,白磷及其完全燃燒的產物的結構如圖Ⅱ所示,則表中x=__________ kJ·mol-1(用含a、b、c、d的代表數式表示)。
查看答案和解析>>
科目: 來源:2016-2017學年四川省高二下學期開學考試化學試卷(解析版) 題型:簡答題
A、B、C、D、E代表前四周期原子序數依次增大的五種元素。A、D同主族且有兩種常見化合物DA2和DA3;工業上電解熔融C2A3制取單質C;B、E除最外層均只有2個電子外,其余各層全充滿,E位于元素周期表的ds區。回答下列問題:
(1)B、C中第一電離能較大的是_________,基態D原子價電子的軌道表達式為____________。
(2)DA2分子的VSEPR模型是____________。H2A比H2D熔沸點高得多的原因是____________。
(3)實驗測得C與氯元素形成化合物的實際組成為C2Cl6,其球棍模型如圖所示。已知C2Cl6 在加熱時易升華,與過量的NaOH溶液反應可生成Na[C(OH)4]。
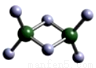
① C2Cl6屬于____________晶體(填晶體類型),其中C原子的雜化軌道類型為____________雜化。
② [C(OH)4]-中存在的化學鍵有___________。
(4)工業上制備B的單質是電解熔融B的氯化物,而不是電解BA,原因是_____________。
(5)B、C的氟化物晶格能分別是2957 kJ·mol-1、5492 kJ·mol-1,二者相差很大的原因是____________。
(6)D與E所形成化合物晶體的晶胞如圖所示。
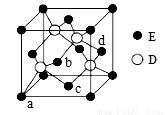
① 在該晶胞中,E的配位數為______________。
② 已知該晶胞的密度為ρ g/cm3,則其中兩個D原子之間的距離為_________ pm(列出計算式即可)。
查看答案和解析>>
科目: 來源:2016-2017學年貴州省凱里市高二下學期開學考試理綜化學試卷(解析版) 題型:選擇題
下列說法正確的是
A. 22.4LO2中一定含有6.02×1023個氧原子
B. 將80gNaOH固體溶于1L水中,所得溶液中NaOH的物質的量濃度為2mol/L
C. 18gH2O在標準狀況下的體積是22.4L
D. 在標況下,20mLNH3與60mLO2所含的分子個數比為1:3
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com