
科目: 來源: 題型:解答題
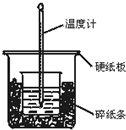 通過測定反應過程中所放出的熱量可計算中和熱.50mL 0.50mol/L鹽酸與50mL 0.55mol/LNaOH溶液在圖示的裝置中進行中和反應.回答下列問題:
通過測定反應過程中所放出的熱量可計算中和熱.50mL 0.50mol/L鹽酸與50mL 0.55mol/LNaOH溶液在圖示的裝置中進行中和反應.回答下列問題:查看答案和解析>>
科目: 來源: 題型:解答題
 利用如圖裝置測定中和熱的實驗步驟如下:
利用如圖裝置測定中和熱的實驗步驟如下:| 溫度 實驗 次數 | 起始溫度t1℃ | 終止溫度t2/℃ | 溫度差平均值 (t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 29.5 | |
| 2 | 27.0 | 27.4 | 27.2 | 32.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.2 | |
| 4 | 26.4 | 26.2 | 26.3 | 29.8 | |
查看答案和解析>>
科目: 來源: 題型:填空題
| 溫度/℃ | 400 | 500 | 830 |
| 平衡常數K | 10 | 9 | 1 |
| 實驗編號 | 反應物投入量 | 平衡時H2濃度 | 吸收或放出的熱量 | 反應物轉化率 |
| A | 1、1、0、0 | c1 | Q1 | α1 |
| B | 0、0、2、2 | c2 | Q2 | α2 |
| C | 2、2、0、0 | c3 | Q3 | α3 |

查看答案和解析>>
科目: 來源: 題型:填空題
| t/s | 0 | 120 | 180 | 240 | 330 | 530 | 600 | 700 | 800 |
| c/mol•L-1 | 0 | 0.036 | 0.030 | 0.026 | 0.022 | 0.017 | 0.016 | 0.015 | 0.015 |
查看答案和解析>>
科目: 來源: 題型:填空題
 (1)化學鍵的鍵能是指氣態原子間形成1mol化學鍵時釋放的能量.下表列出了某些化學鍵的鍵能:
(1)化學鍵的鍵能是指氣態原子間形成1mol化學鍵時釋放的能量.下表列出了某些化學鍵的鍵能:| 化學鍵 | H-H | O═O | O-H |
| 鍵能 (kJ•mol-1) | 436 | x | 463 |
查看答案和解析>>
科目: 來源: 題型:選擇題
 已知:1mol C-H鍵完全斷裂時吸收熱量412kJ,1mol C-C鍵完全斷裂時吸收熱量348kJ1mol C=C鍵完全斷裂吸收熱量612kJ,1mol H-H鍵完全斷裂時吸收熱量436kJ.上述反應的△H等于( ) kJ•mol-1.
已知:1mol C-H鍵完全斷裂時吸收熱量412kJ,1mol C-C鍵完全斷裂時吸收熱量348kJ1mol C=C鍵完全斷裂吸收熱量612kJ,1mol H-H鍵完全斷裂時吸收熱量436kJ.上述反應的△H等于( ) kJ•mol-1.| A. | -124 | B. | +124 | C. | -288 | D. | +288 |
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | 平衡常數減小 | B. | BaO量不變 | C. | 氧氣濃度不變 | D. | 平衡向右移動 |
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | 氯化鎂溶液加熱蒸干最終得不到氯化鎂固體 | |
| B. | 實驗室可用排飽和食鹽水的方法收集氯氣 | |
| C. | 開啟啤酒瓶后,瓶中馬上泛起大量泡沫 | |
| D. | 壓縮氫氣與碘蒸氣反應的平衡混合氣體,顏色變深 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com