
科目: 來源: 題型:解答題

| 編號 | a | b | c | d |
| Ⅰ | 干燥的有色布條 | 干燥的有色布條 | 濕潤的有色布條 | 濕潤的有色布條 |
| Ⅱ | 堿石灰 | 硅膠 | 濃硫酸 | 無水氯化鈣 |
| Ⅲ | 濕潤的有色布條 | 濕潤的有色布條 | 干燥的有色布條 | 干燥的有色布條 |
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | ②③⑦⑧⑨⑩ | B. | ①②③⑤⑧⑨ | C. | ②⑤⑥⑦⑧ | D. | ②④⑦⑧⑩ |
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | 焰火的五彩繽紛是某些金屬元素化學性質的展現 | |
| B. | 將煤氣化后再作為能源,可減少PM2.5引起的危害 | |
| C. | 石英用于生產光導纖維和計算機芯片 | |
| D. | 包裝食品里常有硅膠、石灰、還原鐵粉三類小包,其作用相同 |
查看答案和解析>>
科目: 來源: 題型:解答題
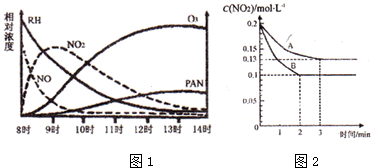
查看答案和解析>>
科目: 來源: 題型:解答題
 某溫度,將2molCO與5molH2的混合氣體充入容積為2L的密閉容器中,在催化劑的作用下發生反應:CO(g)+2H2(g)?CH3OH(g);經過5min后,反應達到平衡,此時轉移電子6mol.
某溫度,將2molCO與5molH2的混合氣體充入容積為2L的密閉容器中,在催化劑的作用下發生反應:CO(g)+2H2(g)?CH3OH(g);經過5min后,反應達到平衡,此時轉移電子6mol.查看答案和解析>>
科目: 來源: 題型:解答題
 氧硫化碳(COS)可替代磷化氫而被用作熏蒸劑.
氧硫化碳(COS)可替代磷化氫而被用作熏蒸劑.查看答案和解析>>
科目: 來源: 題型:解答題
 .
.
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | 3:2:1 | B. | 6:3:2 | C. | 9:3:1 | D. | 12:6:5 |
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | 1gH2和8g O2 | |
| B. | 1molCO和22.4L水蒸氣(一個標準大氣壓、100℃) | |
| C. | 18g水和標況時22.4L CO2 | |
| D. | 3molSO2和2mol SO3 |
查看答案和解析>>
科目: 來源: 題型:解答題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com