
科目: 來源: 題型:解答題
查看答案和解析>>
科目: 來源: 題型:填空題
 .
.| t/K | 300 | 400 | … |
| K/(mol/L)-2 | 4×106 | 8×107 | … |
查看答案和解析>>
科目: 來源: 題型:解答題
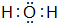 .
. .
.查看答案和解析>>
科目: 來源: 題型:解答題
查看答案和解析>>
科目: 來源: 題型:解答題
查看答案和解析>>
科目: 來源: 題型:解答題
查看答案和解析>>
科目: 來源: 題型:解答題
 A、B、C、D四種元素的核電荷數均小于18,A元素原子核外只有1個電子;B是地殼中含量最多的元素;B、C可形成兩種化合物CB和CB2,C的最高正價與最低負價絕對值相等,CB有毒,CB2可用于滅火;D+具有與Ne原子相同的電子層結構.
A、B、C、D四種元素的核電荷數均小于18,A元素原子核外只有1個電子;B是地殼中含量最多的元素;B、C可形成兩種化合物CB和CB2,C的最高正價與最低負價絕對值相等,CB有毒,CB2可用于滅火;D+具有與Ne原子相同的電子層結構. CB2的電子式為
CB2的電子式為
查看答案和解析>>
科目: 來源: 題型:填空題
查看答案和解析>>
科目: 來源: 題型:多選題
| A. | HF、HCI、HBr、HI的熱穩定性依次減弱 | |
| B. | NaF、NaCl、NaBr、NaI的熔點依次減低 | |
| C. | 金剛石的硬度大于硅,其熔、沸點也高于硅 | |
| D. | F2、Cl2、Br2、I2的熔、沸點逐漸升高 |
查看答案和解析>>
科目: 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com