
科目: 來源: 題型:解答題
 鋰亞硫酰氯(Li-SOCl2)電池具有能量密度高、工作電壓和放電電壓平穩、工作溫度范圍寬及貯存壽命長等優點,在航海、醫療及井下油田設備等方面的應用廣泛.
鋰亞硫酰氯(Li-SOCl2)電池具有能量密度高、工作電壓和放電電壓平穩、工作溫度范圍寬及貯存壽命長等優點,在航海、醫療及井下油田設備等方面的應用廣泛.查看答案和解析>>
科目: 來源: 題型:解答題
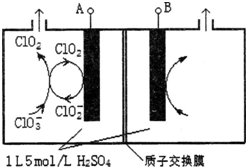 研究含Cl、N、S等元素的化合物對凈化水質、防治污染有重要意義.
研究含Cl、N、S等元素的化合物對凈化水質、防治污染有重要意義.查看答案和解析>>
科目: 來源: 題型:選擇題
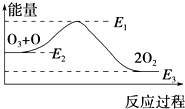 氯原子對O3的分解有催化作用:O3+Cl═ClO+O2△H1,ClO+O═Cl+O2△H2.
氯原子對O3的分解有催化作用:O3+Cl═ClO+O2△H1,ClO+O═Cl+O2△H2.| A. | 反應O3+O═2O2的△H=E1-E3 | B. | 反應O3+O═2O2是吸熱反應 | ||
| C. | △H=△H1+△H2 | D. | 氯原子沒有改變O3分解反應的歷程 |
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | 0.01mol•L-1H2S溶液:c(H+)>c(HS-)>c(S2-)>c(H2S)>c(OH-) | |
| B. | 0.1 mol•L-1NaHSO3溶液:c(Na+)+c(H+)<c(HSO3-)+c(SO32-)+c(OH-) | |
| C. | 等物質的量的NH4Cl和NaCl的混合溶液:c(NH4+)+c(NH3•H2O)+c(Na+)=2c(Cl-) | |
| D. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=10-10的Na2CO3溶液:c(HCO3-)+c(H2CO3)=c(10-2-10-12) mol•L-1 |
查看答案和解析>>
科目: 來源: 題型:選擇題
 向1000mL3mol•L-1NaOH中通入適量CO2氣體,溶液中有關陰離子的物質的量變化曲線如圖所示:下列說法正確的是( )
向1000mL3mol•L-1NaOH中通入適量CO2氣體,溶液中有關陰離子的物質的量變化曲線如圖所示:下列說法正確的是( )| A. | 水的電離程度一直增大 | |
| B. | 溶液的pH逐漸下降 | |
| C. | M、N兩點對應的溶液中離子種類不同 | |
| D. | CD段反應的離子方程式為OH-+CO2=HCO3- |
查看答案和解析>>
科目: 來源: 題型:解答題
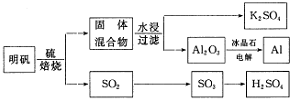
查看答案和解析>>
科目: 來源: 題型:解答題

| 溫度/℃ | 200℃ | 250℃ | 300℃ |
| 平衡常數/(mol•L-1)2 | K1 | K2 | 80 |
查看答案和解析>>
科目: 來源: 題型:解答題
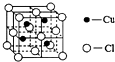 銅是過渡金屬元素,可以形成多種化合物.
銅是過渡金屬元素,可以形成多種化合物.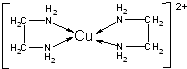
查看答案和解析>>
科目: 來源: 題型:解答題
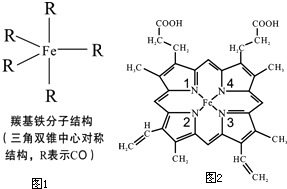 Fe、C、N、O、H可以組成多種物質.回答以下問題:
Fe、C、N、O、H可以組成多種物質.回答以下問題:查看答案和解析>>
科目: 來源: 題型:多選題
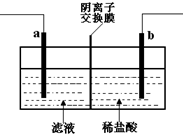 已知陰離子交換膜只允許陰離子通過.某化學課外活動小組采用如下方案對印刷電路廢液(溶質主要是FeCl2、CuCl2和 FeCl3)進行再生:先向廢液中加入過量鐵粉,充分反應后過濾,再將濾液轉入圖所示的裝置中進行電解.下列說法中不正確的是( )
已知陰離子交換膜只允許陰離子通過.某化學課外活動小組采用如下方案對印刷電路廢液(溶質主要是FeCl2、CuCl2和 FeCl3)進行再生:先向廢液中加入過量鐵粉,充分反應后過濾,再將濾液轉入圖所示的裝置中進行電解.下列說法中不正確的是( )| A. | 電解時,電極a應與外電源的正極相連 | |
| B. | 電解時,電極b周圍產生無色無味的氣體 | |
| C. | 電解時,電極a發生的反應是:2Cl--2e-=Cl2↑ | |
| D. | 電解時,可以用氯化鈉溶液替代稀鹽酸 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com