
科目: 來源: 題型:解答題
 實驗小組為探究SO2的漂白性和還原性,設計了以下實驗.
實驗小組為探究SO2的漂白性和還原性,設計了以下實驗.查看答案和解析>>
科目: 來源: 題型:解答題
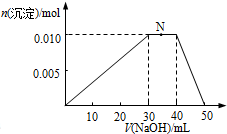 H、C、N、O、Al、S是常見的六種元素.
H、C、N、O、Al、S是常見的六種元素.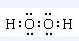 或H:C??C:H.
或H:C??C:H.查看答案和解析>>
科目: 來源: 題型:選擇題
| 選項 | ① | ② | ③ | 實驗結論 |  |
| A | 濃硫酸 | Cu | KMnO4溶液褪色 | SO2有漂白性 | |
| B | 濃鹽酸 | MnO2 | FeBr2溶液變為黃色 | 氧化性:Cl2>Br2 | |
| C | 稀硫酸 | 碳酸鈉 | CaCl2溶液無明顯變化 | CO2不與CaCl2溶液反應 | |
| D | 濃硫酸 | 蔗糖 | 溴水褪色 | 濃硫酸具有脫水性、吸水性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 來源: 題型:選擇題
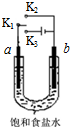 用如圖裝置研究電化學原理,下列分析中錯誤的是( )
用如圖裝置研究電化學原理,下列分析中錯誤的是( )| 選項 | 連接 | 電極材料 | 分析 | |
| a | b | |||
| A | K1 K2 | 石墨 | 鐵 | 模擬鐵的吸氧腐蝕 |
| B | K1 K2 | 鋅 | 鐵 | 模擬鋼鐵防護中犧牲陽極的陰極保護法 |
| C | K1 K3 | 石墨 | 鐵 | 模擬電解飽和食鹽水 |
| D | K1 K3 | 鐵 | 石墨 | 模擬鋼鐵防護中外加電流的陰極保護法 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 來源: 題型:選擇題
 右圖是用點滴板探究氨氣的性質.實驗時向NaOH固體上滴幾滴濃氨水后,立即用培養皿罩住整個點滴板.下列對實驗現象的解釋正確的是( )
右圖是用點滴板探究氨氣的性質.實驗時向NaOH固體上滴幾滴濃氨水后,立即用培養皿罩住整個點滴板.下列對實驗現象的解釋正確的是( )| 選項 | 實驗現象 | 解釋 |
| A | 紅色石蕊試紙變藍 | NH3極易溶于水 |
| B | 濃硫酸附近無白煙 | NH3與濃硫酸不發生反應 |
| C | 氯化鋁溶液變渾濁 | NH3與AlCl3溶液反應:Al3++3OH-→Al(OH)3↓ |
| D | 濃鹽酸附近有白煙 | NH3與揮發出的HCl反應:NH3+HCl→NH4Cl |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 來源: 題型:解答題
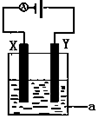 (1)已知H-H 鍵能為436kJ•mol-1,H-N鍵鍵能為391kJ•mol-1,根據化學方程式:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol-1.則N≡N鍵的鍵能是945.6 kJ/mol
(1)已知H-H 鍵能為436kJ•mol-1,H-N鍵鍵能為391kJ•mol-1,根據化學方程式:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol-1.則N≡N鍵的鍵能是945.6 kJ/mol查看答案和解析>>
科目: 來源: 題型:解答題
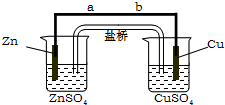 某學生利用下面實驗裝置探究鹽橋式原電池的工作原理.按照實驗步驟依次回答下列問題:
某學生利用下面實驗裝置探究鹽橋式原電池的工作原理.按照實驗步驟依次回答下列問題:查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | 濃硝酸和稀硝酸都具有氧化性 | |
| B. | 濃硝酸與金屬反應不產生氫氣,而稀硝酸與金屬反應可置換出氫氣 | |
| C. | 因常溫下鋁和鐵不與濃硝酸反應,所以濃硝酸可盛放在鋁制或鐵制容器中 | |
| D. | 硝酸與金屬反應時,只表現出氧化性 |
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | 常溫下,濃硫酸與鐵、鋁不反應,所以鐵質、鋁質容器能盛放濃硫酸 | |
| B. | 濃硫酸具有吸水性,故能使蔗糖碳化 | |
| C. | 濃硫酸和銅片加熱既表現出酸性,又表現出氧化性 | |
| D. | 濃H2SO4可做H2、O2等氣體的干燥劑表現其脫水性 |
查看答案和解析>>
科目: 來源: 題型:解答題
 電池的發明和應用是化學家們對人類社會的重要貢獻之一.
電池的發明和應用是化學家們對人類社會的重要貢獻之一.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com