
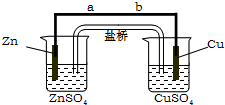
 某學生利用下面實驗裝置探究鹽橋式原電池的工作原理.按照實驗步驟依次回答下列問題:
某學生利用下面實驗裝置探究鹽橋式原電池的工作原理.按照實驗步驟依次回答下列問題:分析 (1)Zn為負極,Cu為正極,電子由負極經導線流向正極;
(2)負極發生氧化反應,Zn失去電子生成鋅離子;
(3)計算Cu的物質的量,結合電極反應式Cu2++2e-=Cu計算轉移電子;
(4)原電池中電解質溶液陰離子向負極移動,陽離子向正向移動;
(5)電解發生2H2O+4AgNO3$\frac{\underline{\;電解\;}}{\;}$4Ag+O2↑+4HNO3 ,向所得溶液中加入23.2g氧化銀,其物質的量為0.1mol,溶液恰好恢復到電解前的狀態,則電解中生成0.2molAg,根據Ag元素化合價變化計算轉移電子.
解答 解:(1)鋅銅原電池中,鋅比銅活潑,Zn與硫酸銅反應生成Cu與硫酸鋅,故鋅為負極,銅為正極,原電池中,電子由負極流向正極,故電子的流向為a→b,故答案為:a→b;
(2)Zn為負極,鋅電極上的電極反應式為 Zn-2e-=Zn2+,故答案為:Zn-2e-=Zn2+;
(3)0.64g銅物質的量為$\frac{0.64g}{64g/mol}$=0.01mol,由電極反應式Cu2++2e-=Cu可知,導線中轉移電子為0.01mol×2=0.02mol,故轉移電子數目為0.02NA,故答案為:0.02NA ;
(4)左側燒杯中鋅失電子變成鋅離子,使得鋅電極附近帶正電荷,吸引陰離子向左側燒杯移動,右側燒杯中銅離子得到電子變成銅,使得銅電極附近帶負電荷,吸引陽離子向右側燒杯移動,故鹽橋中的K+向右側燒杯移動、Cl-向左側燒杯移動,故答案為:B;
(5)電解發生2H2O+4AgNO3$\frac{\underline{\;電解\;}}{\;}$4Ag+O2↑+4HNO3 ,向所得溶液中加入23.2g氧化銀,其物質的量為$\frac{23.2g}{232g/mol}$=0.1mol充分反應后,溶液恰好恢復到電解前的狀態,由Ag原子守恒可知,則電解中生成0.2molAg,則轉移電子的物質的量是0.2mol×(1-0)=0.2mol,故答案為:0.2.
點評 本題主要考查原電池的工作原理、電解原理,關鍵理解掌握原電池與電解工作原理,注意電子轉移守恒再電化學計算中應用,題目難度不大.


科目:高中化學 來源: 題型:選擇題
| A. | 2H2+O2═2H2O | B. | H++OH-═H2O | ||
| C. | .CaCO3═CaO+CO2↑ | D. | Na2CO3+2HCl═2NaCl+H2O+CO2↑ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Na和O2 | B. | Fe和FeCl3 | C. | Na2CO3和HCl | D. | AlCl3和NaOH |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 H、C、N、O、Al、S是常見的六種元素.
H、C、N、O、Al、S是常見的六種元素.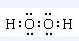 或H:C??C:H.
或H:C??C:H.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 太陽能電池是通過光電效應或者光化學效應直接把光能轉化成電能的裝置.其材料除單晶硅,還有銅銦鎵硒等化合物.
太陽能電池是通過光電效應或者光化學效應直接把光能轉化成電能的裝置.其材料除單晶硅,還有銅銦鎵硒等化合物.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 汽車尾氣是導致酸雨的原因之一 | B. | 酸雨會使土壤、湖泊酸化 | ||
| C. | 酸雨形成中不涉及氧化還原反應 | D. | 燃煤中加入石灰石可防治酸雨 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com