
科目: 來源: 題型:
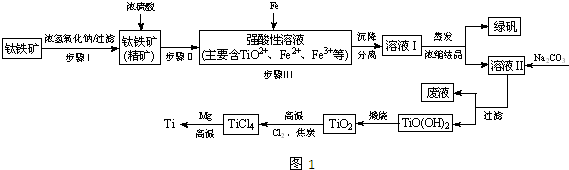
| TiCl4 | Mg | MgCl2 | Ti | |
| 熔點/℃ | -25.0 | 648.8 | 714 | 1667 |
| 沸點/℃ | 136.4 | 1090 | 1412 | 3287 |
查看答案和解析>>
科目: 來源: 題型:
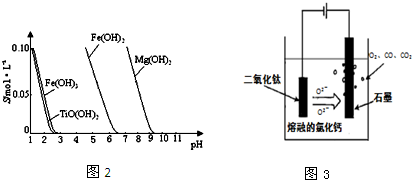
| A、過濾后的溶液中一定沒有S2- |
| B、MnS難溶于水,可溶于MnCl2溶液中 |
| C、常溫時,CuS、PbS、CdS比MnS更難溶 |
| D、加入MnS后生成CuS的離子方程式是Cu2++S2-=CuS↓ |
查看答案和解析>>
科目: 來源: 題型:
| A、離子半徑:O2->Na+>Mg2+ |
| B、堿性:NaOH>Mg(OH)2>Al(OH)3 |
| C、熱穩定性:HCl>PH3>H2S |
| D、結合氫離子能力:CO32->HCO3->SO42- |
查看答案和解析>>
科目: 來源: 題型:
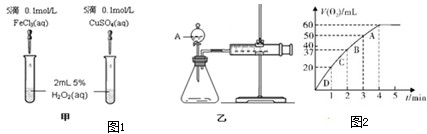
查看答案和解析>>
科目: 來源: 題型:
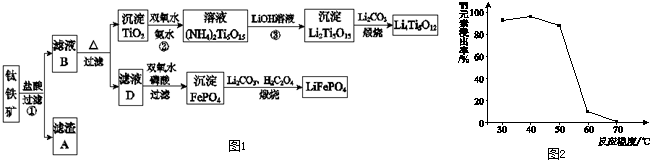
查看答案和解析>>
科目: 來源: 題型:
| ||
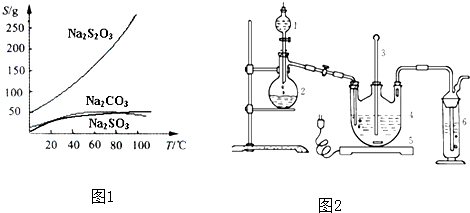
| ||
| 活性炭脫色 |
| 并保溫 |
| 操作① |
| 蒸發濃縮 |
| 冷卻晶體 |
| 操作② |
| 編號 | 1 | 2 | 3 | 4 |
| 消耗Na2S2O3標準溶液的體積/mL | 18.02 | 17.98 | 18.00 | 20.03 |
查看答案和解析>>
科目: 來源: 題型:
A、氘(
| ||||
B、
| ||||
| C、1H2O與2H2O是同一種物質 | ||||
| D、1H218O與2H216O的相對分子質量相同 |
查看答案和解析>>
科目: 來源: 題型:
| A、混合氣體的密度不再發生變化 |
| B、反應過程中v(N2):v(H2)=1:3 |
| C、反應過程中c(N2):c(H2):c(NH3)=1:3:2 |
| D、單位時間內斷開a mol H-H鍵的同時斷開2a mol N-H鍵 |
查看答案和解析>>
科目: 來源: 題型:
 研究NO2、SO2、CO等大氣污染氣體的處理具有重要意義.
研究NO2、SO2、CO等大氣污染氣體的處理具有重要意義.
| ||
| △ |
查看答案和解析>>
科目: 來源: 題型:
| A、混合氣體的壓強不隨時間變化而變化 |
| B、氣體的平均分子量不再變化 |
| C、2 v (B)正=v (D)逆 |
| D、單位時間內消耗n mol C,同時生成2n mol B |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com