

分析 (1)①開始時開關K與a連接形成原電池反應,發生吸氧腐蝕,B電極鐵做負極失電子生成亞鐵離子,A電極石墨做正極溶液中氧氣得到電子生成氫氧根離子;
②開始時開關K與b連接形成電解池,與電源正極相連的A電極為陽極,溶液中氯離子失電子生成氯氣,與電源負極相連的B電極為電解池的陰極,溶液中氫離子得到電子生成氫氣,電解氯化鈉溶液生成氫氧化鈉、氫氣和氯氣;
(2)①陽極氫氧根離子失電子生成氧氣;陰極上氫離子放電,則NaOH在陰極生成;根據陰陽離子的移動方向,通過相同電量時,陰陽離子交換的個數判斷;
②氫氣、氧氣和氫氧化鈉溶液組合為氫氧燃料電池,負極上氫氣失去電子.
解答 解:(1)①開始時開關K與a連接形成原電池反應,發生吸氧腐蝕,A電極石墨做正極溶液中氧氣得到電子生成氫氧根離子,電極反應為:O2+2H2O+4e-=4OH-,
故答案為:吸氧;O2+2H2O+4e-=4OH-;
②開關K與b連接,裝置為電解池,鐵為陰極,發生還原反應,氫離子得到電子生成氫氣,即B電極反應為2H++2e-=H2↑;電解飽和食鹽水生成氫氧化鈉、氫氣和氯氣,電解總反應的離子方程式為2Cl-+2H2O$\frac{\underline{\;通電\;}}{\;}$2OH-+H2↑+Cl2↑,
故答案為:2H++2e-═H2↑;2Cl-+2H2O$\frac{\underline{\;通電\;}}{\;}$2OH-+H2↑+Cl2↑;
(2)①陽極氫氧根離子失電子生成氧氣,則B出口導出的氣體是O2;陰極上氫離子放電,則NaOH在陰極生成,由圖可知,D在陰極附近,制得的氫氧化鈉溶液從D出口導出;陽極氫氧根離子放電,因此硫酸根離子向陽極移動,陰極氫離子放電,因此鈉離子向陰極移動,所以通過相同電量時,通過陰離子交換膜的離子數小于通過陽離子交換膜的離子數,
故答案為:O2;D;<;
②氫氣、氧氣和氫氧化鈉溶液組合為氫氧燃料電池,負極上氫氣失去電子生成水,負極反應式為H2-2e-+2OH-=2H2O,
故答案為:H2-2e-+2OH-=2H2O.
點評 本題考查了原電池和電解池原理,注意裝置的判斷及原電池電極反應式和電解反應的書寫,把握電解質溶液的酸堿性確定生成的離子或物質,題目難度中等,側重于考查學生的分析能力.


 單元期中期末卷系列答案
單元期中期末卷系列答案科目:高中化學 來源: 題型:多選題

| A. | Fe2+、I-、Cl-三種離子一定存在 | |
| B. | 不能確定Na+和Cl-是否存在,CO${\;}_{3}^{2-}$一定不存在 | |
| C. | Fe3+與Fe2+至少有一種 | |
| D. | 該溶液中c(Cl-)≥0.1mol•L-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| ① | ② | ③ | ||
| ④ | ⑤ | ⑥ | ⑦ |
 、
、 ,這兩種離子的半徑大小順序是S2->Cl-(填化學式).
,這兩種離子的半徑大小順序是S2->Cl-(填化學式).查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 溫度/℃ | 1000 | 1115 | 1300 |
| 平衡常數 | 4.0 | 3.7 | 3.5 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
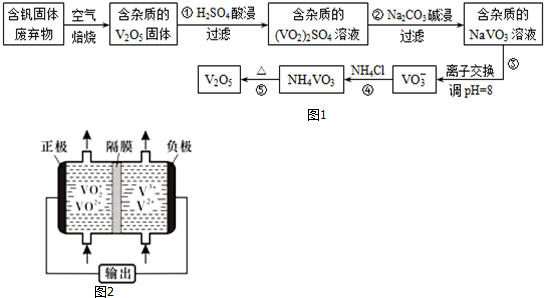
| 物質 | V2O5 | NH4VO3 | VOSO4 | (VO2)2SO4 |
| 溶解性 | 難溶 | 難溶 | 可溶 | 易溶 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 | 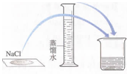 |  | 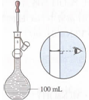 |
| A.接近稱量質量時,輕振手腕,加夠藥品 | B.溶解時,用量筒控制所加蒸餾水的量 | C.移液時,玻璃棒插在刻度線以上,防止液體灑出 | D.接近刻度線1~2 cm時,用膠頭滴管滴加蒸餾水至刻度線 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 所需儀器有:100mL容量瓶、燒杯、玻璃棒、膠頭滴管、托盤天平 | |
| B. | 將量取的濃鹽酸先倒入容量瓶,再加入蒸餾水至刻度線,搖勻 | |
| C. | 將溶液轉移入容量瓶,要用玻璃棒引流 | |
| D. | 定容時仰視刻度,所配溶液濃度偏小 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 某氣體$\stackrel{通入品紅溶液中}{→}$品紅溶液褪色 結論:某氣體一定是SO2 | |
| B. | 某氣體$\stackrel{通入澄清石灰水}{→}$ 產生白色沉淀 結論:某氣體一定是CO2 | |
| C. | 某溶液$\stackrel{打開瓶蓋}{→}$冒白霧$\stackrel{將沾有濃氨水的玻璃棒靠近}{→}$ 白煙 結論:原溶液一定是濃鹽酸 | |
| D. | 某溶液$\stackrel{滴加KSCN溶液液}{→}$ 血紅色溶液 結論:原溶液中一定含有Fe3+ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
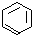 、④HCHO,其中碳原子采取sp2雜化的分子有①③④(填物質編號),HCHO分子的立體構型為平面三角形.
、④HCHO,其中碳原子采取sp2雜化的分子有①③④(填物質編號),HCHO分子的立體構型為平面三角形.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com