
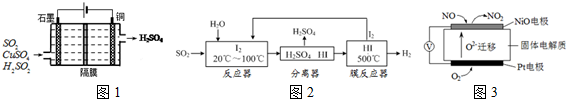
分析 (1)①二氧化硫是一種有毒的氣體,排放到空氣中可引起酸雨的發生,對環境和人類健康有害,脫硫可以防止酸雨的發生;
依據二氧化硫和氧氣反應方程式,找出二氧化硫和氧氣量的關系;
②利用電解原理將二氧化硫轉化成硫酸吸收,先寫出兩個電極上上發生的電極反應式,加和就可得到總的離子方程式.
(2)①從流程圖可知,在反應器中,I2氧化SO2,生成硫酸和HI;
②HI分解是可逆反應,分離出氫氣有利于平衡正向移動.
Ⅱ.由離子的定向移動可知NiO極為原電池的負極,Pt極為原電池的正極,正極發生還原反應,負極發生氧化反應,以此解答該題.
解答 解;(2)①脫硫可以減少二氧化硫的排放量,防止酸雨的發生,2SO2 +O2 =2SO3
2mol 32g
故答案為:防止酸雨的發生;32;
②分析圖中電解裝置,可知左邊石墨是電解池的陽極,右邊是電解池的陰極;
陽極放電的物質二氧化硫,失去電子生成硫酸根離子,電極反應式:SO2-2e-+2H2O=SO42-+2H+;
陰極放電的物質時銅離子,得到電子被還原成單質銅,電極反應式:Cu2++2e-=Cu;
將上述兩電極的電極反應式得:SO2+2H2O+Cu2+$\frac{\underline{\;通電\;}}{\;}$4H++SO42-+Cu,
故答案為:SO2+2H2O+Cu2+$\frac{\underline{\;通電\;}}{\;}$4H++SO42-+Cu.
(2)①從流程圖可知,在反應器中,I2氧化SO2,生成硫酸和HI,反應方程式為SO2+I2+2H2O=SO42-+2I-+4H+,故答案為:SO2+I2+2H2O=SO42-+2I-+4H+;
②HI分解為可逆反應,及時分離出產物H2,有利于反應正向進行,故答案為:HI分解為可逆反應,及時分離出產物H2,有利于反應正向進行.
Ⅱ.由離子的定向移動可知NiO極為原電池的負極,負極反應為NO-2e-+O2-=NO2,pt電極上電極反應為O2+4e-=2O2-,則電池中每轉移0.4mol e-,Pt電極消耗氧氣為0.1mol×22.4L/mol=2.24L,故答案為:2.24;NO-2e-+O2-=NO2.
點評 本題考查氧化還原反應及電化學知識,為高考常見題型和高頻考點,注意把握原電池的工作原理,本題解答的關鍵是離子的定向移動,以此可確定電源的兩極和反應類型,注意體會答題思路,題目難度中等.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題
| A. | 同一反應中,氧化劑失電子的總數一定等于還原劑得電子的總數 | |
| B. | 氧化劑在反應中被還原,生成氧化產物 | |
| C. | 氧化還原反應的特征是有化合價的升降 | |
| D. | 任何反應中一定有氧化劑和還原劑,且氧化劑和還原劑必須為不同種物質 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 實驗序號 | 甲 | 乙 | 丙 |
| 鹽酸體積/mL | 300 | 300 | 300 |
| 合金質量/g | 5.1 | 7.65 | 9.18 |
| 生成氣體體積/L | 5.6 | 6.72 | 6.72 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 4g D2和足量O2反應可生成D2O的分子數目為2NA | |
| B. | 0.1molCl2與足量NaOH溶液反應,轉移電子的數目為0.2NA | |
| C. | 在標準狀況下,2.24L氨氣所含的電子總數為NA | |
| D. | 標準狀況下,6.4 g氧氣和臭氧中含有的分子總數為0.2 NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 體積之比為2:1 | B. | 原子總數之比為1:2 | ||
| C. | 物質的量之比為1:1 | D. | 氧原子的個數之比為1:1 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com