

| CO | H2O | CO2 | H2 |
| 0.5mol | 8.5mol | 2.0mol | 2.0mol |
分析 (1)①平衡狀態是正逆反應速率相同,各組分含量保持不變,物質濃度不變,依據圖形中甲烷的濃度變化曲線分析判斷平衡狀態;10min時,甲烷濃度減小,說明平衡正向進行,反應是吸熱反應,則改變的外界條件可能是升溫;
②甲為恒溫恒容容器,乙為恒溫恒壓容器,乙容器中隨反應進行,氣體體積增大,為保持恒壓,體積增大,壓強減小,平衡正向進行;
(2)計算此時的濃度商和平衡常數比較來判斷反應是否達到平衡狀態;
(3)①合成氨的反應是放熱反應,開始反應,氨氣物質的量增大,達到平衡狀態,繼續升溫,平衡逆向進行,氨氣物質的量減小,據此畫出變化圖象;
②依據反應是氣體體積減小的放熱反應,結合平衡移動原理分析判斷;
解答 解:(1)①分析CH4的物質的量濃度隨反應時間的變化可知,濃度在5~10分鐘、12分鐘后 曲線出現平臺,說明濃度不變,反應達到平衡狀態,反應是吸熱反應,在10min甲烷濃度減小最后達到平衡狀態,說明改變的條件可以是升高溫度,平衡正向進行,
故答案為:5~10分鐘、12分鐘后,升高溫度;
②在初始容積相等的甲、乙兩容器中分別充入等物質的量的CH4和H2O.在相同溫度下發生反應,并維持反應過程中溫度不變,甲為恒溫恒容容器,乙為恒溫恒壓容器,乙容器中隨反應進行,氣體體積增大,為保持恒壓,體積增大,壓強減小,平衡正向進行,甲烷的轉化率增大,故α甲(CH4)<α乙(CH4),
故答案為:<;
(2)CO(g)+H2O(g)?CO2(g)+H2(g),一定溫度下,反應的平衡常數為K=1.某時刻測得該溫度下的密閉容器中各物質的物質的量,反應前后氣體物質的量不變,可以利用物質的量代替濃度計算反應的濃度商Qc=$\frac{2×2}{0.8×8.5}$=0.6<K=1,則反應正向進行,選a,
故答案為:a;
(3)①合成氨的反應是放熱反應,反應達到一定溫度才可以發生反應,開始反應,氨氣物質的量增大,達到平衡狀態,繼續升溫,平衡逆向進行,氨氣物質的量減小,畫出的圖象為: ,故答案為;
,故答案為; ;
;
②依據平衡移動原理分析,分離出氨氣促進平衡正向進行,反應時氣體體積減小的反應,增大壓強也可以使平衡正向進行,反應是放熱反應,降低溫度會使平衡正向進行,提高反應物的轉化率,
故答案為:增大壓強或降低溫度或分離液氨;
點評 本題考查了化學平衡影響因素分析,平衡計算應用,注意反應特征的計算應用,圖象繪制,掌握基礎是關鍵,題目難度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.02 mol/(L•s) | B. | 3.6 mol/(L•s) | C. | 1.2 mol/(L•s) | D. | 0.04mol/(L•s) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
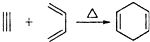 ,如果要合成
,如果要合成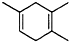 所用的原始原料可以是( )
所用的原始原料可以是( )| A. | 只有① | B. | ②③ | C. | ②④ | D. | ①④ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 3:11 | B. | 11:3 | C. | 2:3 | D. | 4:3 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 ),是由五個苯環相連形成的.下列有關奧林匹克烴的說法正確的是( )
),是由五個苯環相連形成的.下列有關奧林匹克烴的說法正確的是( )| A. | 該有機物屬于芳香族化合物,是苯的同系物 | |
| B. | 能與溴水發生加成反應 | |
| C. | 能使酸性高錳酸鉀溶液褪色 | |
| D. | 該烴的分子式為C22H14 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| 序號 | 實驗內容 | 實驗目的 |
| A | 在滴有酚酞的Na2CO3溶液中,滴加入BaC12溶液,溶液紅色逐漸褪去 | 證明Na2CO3溶液中存在水解平衡 |
| B | 將Al泊插入濃硝酸中,無現象 | 證明Al和濃硝酸不反應 |
| C | 將兩個完全相同且充滿NO2的密閉燒瓶,分別浸泡于熱水、冰水中 | 探究溫度對化學平衡狀態的影響 |
| D | 向同體積同濃度的H2O2溶液中,分別加入1mL同濃度的CuSO4、FeCl3溶液 | 比較Cu2+、Fe3+對H2O2分解速率的影響 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

| 沉淀物 | Fe(OH)3 | Fe(OH)2 | AlOH)3 |
| 開始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com