
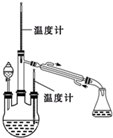
 肼是重要的化工原料.某研究小組利用下列反應制取水合肼(N2H2•H2O):CO(NH2)+2NaOH+NaClO=Na2CO3+N2H4•H2O+NaCl
肼是重要的化工原料.某研究小組利用下列反應制取水合肼(N2H2•H2O):CO(NH2)+2NaOH+NaClO=Na2CO3+N2H4•H2O+NaCl分析 (1)氯氣通入到盛有NaOH的錐形瓶中發生反應生成氯化鈉、次氯酸鈉和水;
(2)由N2H4•H2O+2NaClO=N2↑+3H2O+2NaCl,可知水合肼(N2H4•H2O)具有還原性,易被次氯酸鈉氧化;
(3)水合肼與碘溶液反應發生氧化還原反應,生成氮氣、碘化氫和水;NaHCO3能控制溶液的pH在6.5左右,是因為碳酸氫鈉和碘化氫反應;
(4)碘水具有強氧化性,能腐蝕堿式滴定管的橡膠;根據方程式計算水合肼的物質的量,進而計算其質量分數.
解答 解:(1)氯氣通入到盛有NaOH的錐形瓶中發生反應生成氯化鈉、次氯酸鈉和水,反應的離子方程式為:Cl2+2OH-=ClO-+Cl-+H2O;
故答案為:Cl2+2OH-=ClO-+Cl-+H2O;
(2)由N2H4•H2O+2NaClO=N2↑+3H2O+2NaCl,可知水合肼(N2H4•H2O)具有還原性,如果次氯酸鈉溶液裝在燒瓶中,反應生成的水合肼會被次氯酸鈉氧化,故分液漏斗中的溶液是NaOH和NaClO混合溶液,
故答案為:A;如果次氯酸鈉溶液裝在燒瓶中,反應生成的水合肼會被次氯酸鈉氧化;
(3)水合肼與碘溶液反應發生氧化還原反應,生成氮氣、碘化氫和水,反應的化學方程式為:N2H4•H2O+2I2=N2↑+4HI+H2O;NaHCO3能控制溶液的pH在6.5左右,是因為碳酸氫鈉和碘化氫反應;
故答案為:N2H4•H2O+2I2=N2↑+4HI+H2O;生成的HI與NaHCO3反應;
(4)碘單質具有氧化性,能腐蝕堿式滴定管的橡膠,則碘水應裝在酸式滴定管中;
N2H4•H2O+2I2=N2↑+4HI+H2O;
1 2
n 0.2000mol/L×0.018L
n=0.0018mol
250ml溶液中含有的物質的量=0.0018mol×$\frac{250mL}{25mL}$=0.018mol,
水合肼(N2H4•H2O)的質量分數=$\frac{0.018mol×50g/mol}{5.00g}$×100%=18.0%
故答案為:酸式;18.0%.
點評 本題考查了物質制備實驗、物質含量測定、元素化合物性質、滴定應用等,注意對基礎知識的理解與靈活應用,題目難度中等.


 一線名師提優試卷系列答案
一線名師提優試卷系列答案科目:高中化學 來源: 題型:解答題
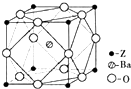 A、B、X、Y、Z為周期表前四周期元素,原子序數依次遞增.已知:
A、B、X、Y、Z為周期表前四周期元素,原子序數依次遞增.已知:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
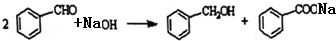
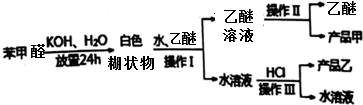
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 4個 | B. | 5個 | C. | 6個 | D. | 7個 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 工業上主要采用氨氧化法生產硝酸,如圖是氨氧化率與氨-空氣混合氣中氧氨比的關系.其中直線表示反應的理論值;曲線表示生產實際情況.當氨氧化率達到100%,理論上r$\frac{n({O}_{2})}{n(N{H}_{3})}$=1.25,實際生產要將r值維持在1.7~2.2之間,原因是O2太少不利于NH3的轉化,r值為2.2時NH3氧化率已近100%.
工業上主要采用氨氧化法生產硝酸,如圖是氨氧化率與氨-空氣混合氣中氧氨比的關系.其中直線表示反應的理論值;曲線表示生產實際情況.當氨氧化率達到100%,理論上r$\frac{n({O}_{2})}{n(N{H}_{3})}$=1.25,實際生產要將r值維持在1.7~2.2之間,原因是O2太少不利于NH3的轉化,r值為2.2時NH3氧化率已近100%.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
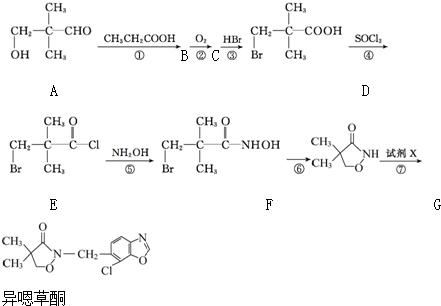
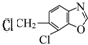 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
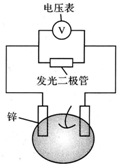 留心處處皆學問.從生活出發進行科學探究,可以獲得自信,形成正確的思維方式.甲、乙兩位同學一起合作設計完成了水果電池的實驗(如圖),測得數據如下
留心處處皆學問.從生活出發進行科學探究,可以獲得自信,形成正確的思維方式.甲、乙兩位同學一起合作設計完成了水果電池的實驗(如圖),測得數據如下| 實驗序號 | 電極材料 | 水果種類 | 電極間距離/cm | 電壓/mV |
| 1 | 鋅銅 | 菠蘿 | 3 | 900 |
| 2 | 鋅銅 | 蘋果 | 3 | 650 |
| 3 | 鋅銅 | 柑橘 | 3 | 850 |
| 4 | 鋅銅 | 西紅柿 | 3 | 750 |
| 5 | 鋅鋁 | 菠蘿 | 3 | 650 |
| 6 | 鋅鋁 | 蘋果 | 3 | 450 |
| 甲同學 | 乙同學 | |
| A | 實驗6中負極電極反應式如何寫? | Al-3e-=Al3+ |
| B | 實驗1,5中電流方向為什么相反? | 1中鋅為負極,電流由銅經導線流向鋅,5中鋁為負極,鋁失去電子,電流由鋅經導線流向鋁 |
| C | 水果電池的電壓與哪些因素有關? | 只跟水果的類型有關 |
| D | 實驗中發光二極管不亮,如何使它亮起來 | 可用銅鋅作電極,用菠蘿作介質,并將多個此電池串聯起來 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com