

 )分子中有5n個σ鍵
)分子中有5n個σ鍵| 化學鍵 | Si-Si | O═O | Si-O |
| 鍵能(kJ•mol-1) | a | b | c |
分析 (1)鐵是26號元素,基態原子核外有26個電子,3d、4s能級上電子是其價電子,根據構造原理書寫其基態價電子排布式;
(2)根據價層電子對互斥理論確定離子空間構型,原子個數相等價電子數相等的微粒是等電子體,正負電荷重心重合的分子是非極性分子;
(3)根據價層電子對互斥理論確定碳原子雜化方式;
(4)a氫鍵的存在影響物質的熔沸點;
b根據化合物中化合價的代數和為0計算;
c聚乙烯(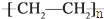 )分子中有(6n-1)個σ鍵;
)分子中有(6n-1)個σ鍵;
d.60gSiO2的物質的量=$\frac{60}{60}$,一個硅原子含有4個硅氧鍵;
(5)鐵和氨氣在640℃可發生置換反應生成氫氣和氮化鐵,利用均攤法確定氮化鐵的化學式,根據溫度、反應物和生成物寫出反應方程式;
設正四面體的棱長為xcm,則正四面體的面對角線為$\sqrt{2}$xcm,又兩個最近的Fe原子間的距離為scm,所以$\frac{\sqrt{2}}{2}$x=s,則x=$\sqrt{2}$scm,根據ρ=$\frac{m}{V}$計算晶胞密度.
解答 解:(1)鐵是26號元素,基態原子核外有26個電子,3d、4s能級上電子是其價電子,根據構造原理知其價電子排布式為:3d64s2,故答案為:3d64s2;
(2)NO3-中N原子價層電子對=3+$\frac{1}{2}$(5+1-3×2)=3,且不含孤電子對,所以是平面三角形結構,
與N03-互為等電子體的一種非極性分子有:BF3[SO3( g)、BBr3等],
故答案為:平面正三角形,BF3[SO3( g)、BBr3等];
(3)只要共價單鍵和孤電子對的和是4的原子就采取sp3雜化,根據圖片知,采用sp3雜化的原子有C、N、O、S,故答案為:C、N、O、S;
(4)a.乙醇分子間可形成氫鍵,氯乙烷中不含氫鍵,氫鍵的存在導致乙醇的沸點升高,所以乙醇的沸點比氯乙烷高,故正確;
b.根據化合物中化合價的代數和為0知,鎢的配合物離子[W(CO)5OH]-中鎢顯0價,故錯誤;
c.聚乙烯(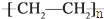 )分子中有(6n-1)個σ鍵,故錯誤;
)分子中有(6n-1)個σ鍵,故錯誤;
d.由表中數據知反應Si(s)+O2(g)=SiO2(s)中,每生成60gSiO2放出的能量為(4c-2a-b)kJ,故錯誤;
故選a;
(5)該晶胞中鐵原子個數=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,氮原子個數是1,所以氮化鐵的化學式是Fe4N,鐵和氨氣在640℃可發生置換反應生成氫氣和氮化鐵,所以該反應方程式為:8Fe+2NH3$\frac{\underline{\;640℃\;}}{\;}$2Fe4N+3H2,
設正四面體的棱長為xcm,則正四面體的面對角線為$\sqrt{2}$xcm,又兩個最近的Fe原子間的距離為scm,所以$\frac{\sqrt{2}}{2}$x=s,則x=$\sqrt{2}$scm,根據ρ=$\frac{m}{V}$=$\frac{\frac{56×4+14}{N{\;}_{A}}}{(\sqrt{2}s){\;}^{3}}$=$\frac{{119\sqrt{2}}}{{2{s^3}{N_A}}}$.
故答案為:8Fe+2NH3$\frac{\underline{\;640℃\;}}{\;}$2Fe4N+3H2;$\frac{{119\sqrt{2}}}{{2{s^3}{N_A}}}$.
點評 本題考查較綜合,電子數排布式的書寫、雜化方式的判斷、晶胞的計算都是學習重點,難點是(4)cd選項,c選項中利用數學歸納法分析,d選項中明確硅、二氧化硅的空間結構是解此選項是關鍵,難度中等.


科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ③④ | B. | ①③ | C. | ①② | D. | ①③④ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用碳酸鈉溶液吸收少量二氧化硫:2CO32-+SO2+H2O═2HCO3-+SO32- | |
| B. | 向碳酸氫鈉溶液中加入氫氧化鈉:HCO3-+OH-═CO2↑+H2O | |
| C. | 向FeCl3溶液中加入銅片:Fe3++Cu═Fe2++Cu2+ | |
| D. | 向NaHSO4溶液中滴加過量Ba(OH)2溶液:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 大理石與鹽酸反應:CaCO3+2H+=Ca2++H2O+CO2↑ | |
| B. | 少量金屬鈉放入冷水中:Na+2H2O=Na++2OH-+H2↑ | |
| C. | 二氧化硅與苛性鈉溶液反應:SiO2+2OH-=SiO${\;}_{3}^{2-}$+H2O | |
| D. | 澄清石灰水通入過量CO2的總反應:CO2+OH-=HCO${\;}_{3}^{-}$ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 常溫常壓下,氯氣呈氣態而溴單質呈液態 | |
| B. | 硝酸是揮發性酸,硫酸是難揮發性的酸 | |
| C. | 稀有氣體一般難發生化學反應 | |
| D. | 氮氣在常溫下很穩定,化學性質不活潑 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 實驗內容 | 結論 |
| A | 某物質的水溶液能使紅色石蕊試紙變藍 | 該物質一定是氨氣 |
| B | 某物質的水溶液中加入鹽酸產生無色無味氣體 | 該溶液一定含有大量碳酸根離子 |
| C | 測定同濃度Na2CO3 和Na2SO4 溶液的pH,前者大于后者 | 碳元素非金屬性弱于硫 |
| D | 向沸水中逐滴加入1~2mL FeCl3飽和溶液,攪拌并繼續煮沸出現渾濁 | 制備Fe(OH)3膠體 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | SO2氧化性比I2強 | |
| B. | 還原性:I->SO2>Cl- | |
| C. | Cl2能氧化I-和SO2 | |
| D. | 最后溶液中溶液一定含有Cl-、SO42-和I2 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com