
| A. | 125 mL | B. | 275 mL | C. | 325 mL | D. | 450 mL |
分析 20mL 1mol/L的AlCl3溶液中氯化鋁的物質的量=0.02L×1mol/L=0.02mol,若Al元素都轉化為氫氧化鋁沉淀,則氫氧化鋁沉淀的質量=0.02mol×78g/mol=1.56g>1.17g,說明有兩種情況:一為沉淀不完全,只生成Al(OH)3沉淀;另一種情況為沉淀部分溶解,既生成Al(OH)3沉淀,又生成NaAlO2,結合方程式計算消耗氫氧化鈉物質的量,進而計算需要氫氧化鈉溶液體積.
解答 解:20mL 1mol/L的AlCl3溶液中氯化鋁的物質的量=0.02L×1mol/L=0.02mol,若Al元素都轉化為氫氧化鋁沉淀,則氫氧化鋁沉淀的質量=0.02mol×78g/mol=1.56g>1.17g,說明有兩種情況:一為沉淀不完全,只生成Al(OH)3沉淀;另一種情況為沉淀部分溶解,既生成Al(OH)3沉淀,又生成NaAlO2.
n(Al(OH)3)=$\frac{1.17g}{78g/mol}$=0.015mol,
①若堿不足,由Al3++3OH-═Al(OH)3↓可知,
NaOH的物質的量為0.015mol×3=0.045mol,
加入NaOH溶液的體積為$\frac{0.045mol}{0.2mol/L}$=0.225L=225mL;
②沉淀部分溶解,既生成Al(OH)3沉淀,又生成NaAlO2,則:
Al3++3OH-═Al(OH)3↓
0.02mol 0.06mol 0.02mol
溶解的氫氧化鋁為0.02mol-0.015mol=0.005mol
Al(OH)3 +OH-═AlO2-+2H2O
0.005mol 0.005mol
則消耗的堿的物質的量為0.06mol+0.005mol=0.065mol,
加入NaOH溶液的體積為$\frac{0.065mol}{0.2mol/L}$=0.325L=325mL;
故選C.
點評 本題考查方程式的有關計算,題目難度中等,關鍵是根據氯化鋁與氫氧化鋁的量判斷發生的反應,再結合反應的有關方程式計算.


 互動英語系列答案
互動英語系列答案科目:高中化學 來源: 題型:選擇題
| A. | ②③⑥ | B. | ②⑤ | C. | ③⑤⑥ | D. | ④⑥ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 該反應中肼作還原劑 | |
| B. | 液態肼的燃燒熱△H為-641.6kJ•mol-1 | |
| C. | 該動力源的突出優點之一是生成物對環境污染小 | |
| D. | 肼和過氧化氫反應的熱化學方程式為:N2H4(l)+2H2O2(l)═N2(g)+4H2O(g);△H=-641.6kJ•mol-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 銅片接電源的正極 | |
| B. | 銅片上發生的反應是:Ag++e-═Ag | |
| C. | 銀片上發生的反應是:4OH--4e-═O2↑+2H2O | |
| D. | 需用硫酸銅溶液為電鍍液 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
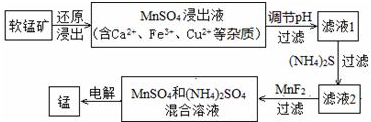
| 物質 | Fe(OH)3 | Cu(OH)2 | Ca(OH)2 | Mn(OH)2 | CuS | CaS | MnS | MnCO3 |
| pKsp | 37.4 | 19.32 | 5.26 | 12.7 | 35.2 | 5.86 | 12.6 | 10.7 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 向稀HNO3中滴加Na2SO3溶液SO32-+2H+═SO2↑+H2O | |
| B. | CuSO4溶液與H2S反應的離子方程式:Cu2++S2-═CuS↓ | |
| C. | 氯氣溶于水:Cl2+H2═2H++Cl-+ClO- | |
| D. | 向CuSO4溶液中加入Na2O2:2Na2O2+2Cu2++2H2═4Na++2Cu(OH)2↓+O2↑ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com