

分析 (1)根據蓋斯定律來計算化學反應的焓變,反應能自發進行,應滿足△H-T•△S<0;
(2)表示平衡常數Kp時用氣體組分(B)的平衡壓強p(B)代替該氣體物質的量的濃度c(B),可根據平衡常數的表達式書寫,平衡常數等于氣體生成物濃度冪之積除以氣體反應物濃度冪之積;
(3)①依據圖象分析解答即可;
②根據圖示內容對比260℃時SO2的轉化率來尋找反應速率最快,根據催化劑和二氧化硫轉化率之間的關系來判斷Fe2O3作催化劑的優點;
(4)n(CO):n(SO2)=2:1時反應速率界于n(CO):n(SO2)=3:1和n(CO):n(SO2)=1:1之間,壓強對反應速率的影響來回答即可;
(5)由反應可知吸收二氧化硫的反應為放熱反應,則高溫下不利于吸收二氧化硫.
解答 解:(1)已知①2CO(g)+O2(g)=2CO2(g)△H1=-566kJ•mol-1②S(l)+O2(g)=SO2(g)△H2=-296kJ•mol-1反應2CO(g)+SO2(g)$\stackrel{催化劑}{?}$2CO2(g)+S(l)可以是①-②所得,所以該反應的焓變:a=-566-(-296)=-270,由于此反應為熵減的過程,即△S<0,若能自發進行,應△H-T•△S<0,溫度不易過高,
故答案為:-270;低溫下進行;
(2)反應I的Kp=$\frac{{p}^{2}(C{O}_{2})}{{p}^{2}(CO)•p(S{O}_{2})}$,故答案為:$\frac{{p}^{2}(C{O}_{2})}{{p}^{2}(CO)•p(S{O}_{2})}$;
(3)①A、依據圖象可知:260℃時氧化鉻的催化效果最好,即二氧化硫的轉化率最高,與速率無關,故A錯誤;
B、380℃時,Fe2O3作催化劑時SO2平衡轉化率接近100%,達到最大,故B正確;
C、反應I為放熱反應,溫度越高,越不利于二氧化硫的轉化,故C錯誤;
D、反應I為放熱反應,溫度不變時,反應達到平衡,故D正確,
故選BD;
②根據圖示內容,對比260℃時不同催化劑作用下SO2的轉化率,可以看出Cr2O3作催化劑時,反應速率最快,Fe2O3和NiO作催化劑均能使SO2的轉化率達到最高,但是Fe2O3作催化劑時,在相對較低溫度可獲得較高SO2的轉化率,從而節約大量能源,
故答案為:Fe2O3作催化劑時,在相對較低溫度可獲得較高SO2的轉化率,從而節約大量能源;
(4)n(CO):n(SO2)=2:1時反應速率界于n(CO):n(SO2)=3:1和n(CO):n(SO2)=1:1之間,反應速率介于二者之間,且二氧化硫的轉化率和n(CO):n(SO2)=3:1是相等的,即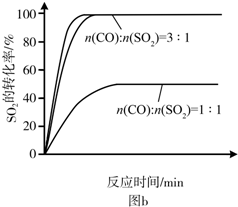 ,故答案為:
,故答案為: ;
;
(5)Na2SO3(aq)+SO2(g)+H2O(l)?2NaHSO3(aq)△H<0,此反應特點為氣體體積增大的放熱反應,故降低溫度,有利于二氧化硫的吸收,增大壓強有利于二氧化硫的吸收,故答案為:降溫、加壓.
點評 本題考查學生有關熱化學、化學反應速率、弱電解質的電離等方面的知識,屬于綜合知識的考查,難度較大.


 通城學典默寫能手系列答案
通城學典默寫能手系列答案 金牌教輔培優優選卷期末沖刺100分系列答案
金牌教輔培優優選卷期末沖刺100分系列答案科目:高中化學 來源: 題型:選擇題
| A. | 含有NA個氮原子的氮氣在標準狀況下的體積約為11.2L | |
| B. | 25℃,1.01×105Pa,64gSO2中含有的原子數小于3NA | |
| C. | 在常溫常壓下,11.2L Cl2含有的分子數為0.5NA | |
| D. | 1 mo1 Na2O2與足量H2O反應,轉移了2 NA 個電子 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 5.6L | B. | 11.2L | C. | 16.8L | D. | 22.4L |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 木材纖維和土豆淀粉遇碘水均顯藍色 | |
| B. | 食用花生油和雞蛋清都能發生水解反應 | |
| C. | 包裝用材料聚乙烯和聚氯乙烯都屬于烴 | |
| D. | PX項目的主要產品對二甲苯屬于飽和烴 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

| t/min | 0 | 2.0 | 4.0 | 6.0 | 8.0 |
| n(Cl2)/10-3mol | 0 | 1.8 | 3.7 | 5.4 | 7.2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

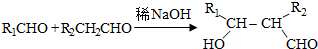
 .
. .
.
 (寫結構簡式)
(寫結構簡式)查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 液晶態介于晶體狀態和液態之間,液晶具有一定程度的晶體的有序性和液體的流動性 | |
| B. | 常壓下,0℃時冰的密度比水的密度小,水在4℃時密度最大,這些都與分子間的氫鍵有關 | |
| C. | 石油裂解、煤的干餾、玉米制醇、蛋白質的變性和納米銀粒子的聚集都是化學變化 | |
| D. | 燃料的脫硫脫氮、SO2的回收利用和NOx的催化轉化都是減少酸雨產生的措施 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com