
| A、0.1mol的白磷(P4)或四氯化碳(CCl4)中所含的共價鍵數均為0.4NA |
| B、1L amol/L的氯化鐵溶液中,若Fe3+的數目為NA,則Cl-的數目為3NA |
| C、0.1 molN2和0.3molH2在一定條件下充分反應,轉移電子數目為0.6NA |
| D、常溫常壓下,65gZn與足量濃 H2SO4充分反應,轉移電子數一定為2NA |


 七彩題卡口算應用一點通系列答案
七彩題卡口算應用一點通系列答案科目:高中化學 來源: 題型:
A、一種鎂電池的反應式為XMg+Mo3S4
| |||
| B、在復鹽NH4Fe(SO4)2溶液中逐滴加入Ba(OH)2溶液,可能發生的反應的離子方程式是NH4++Fe3++2SO42-+2Ba2++4OH-=2BaSO4↓+Fe(OH)3↓+NH3?H2O | |||
| C、在甲、乙兩個體積不變且相同的密閉容器中發生反應A(g)+2B(g)?2C(g),初始條件均為:常溫,A、B兩氣體各1mol.甲容器中的反應在常溫下達平衡,此時氣體壓強為原來氣體壓強的80%,乙容器中的反應在200℃時達平衡,若此時氣體A的體積分數為35% 則說明該反應是放熱反應 | |||
| D、已知:N2(g)+2O2(g)=2NO2(g)△H=+68 kJ?mol-12C(s)+O2(g)=2CO(g)△H=-221 kJ?mol-1C(s)+O2(g)=CO2(g)△H=-393.5 kJ?mol-1則4CO(g)+2NO2(g)=4CO2(g)+N2(g)△H=-1200 kJ?mol-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:

| 過程Ⅳ,B溶液中含有的離子 | 過程Ⅵ,B溶液中 含有的離子 | |
| 甲 | 有Fe3+無Fe2+ | 有SO |
| 乙 | 既有Fe3+又有Fe2+ | 有SO |
| 丙 | 有Fe3+無Fe2+ | 有Fe2+ |
查看答案和解析>>
科目:高中化學 來源: 題型:
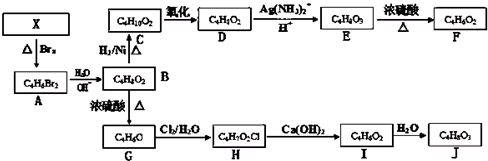
查看答案和解析>>
科目:高中化學 來源: 題型:
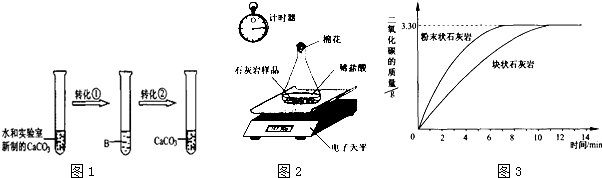
查看答案和解析>>
科目:高中化學 來源: 題型:
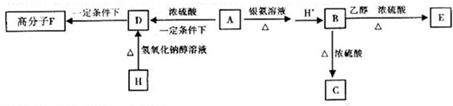
查看答案和解析>>
科目:高中化學 來源: 題型:
| 錐形瓶中溶液 | 滴定管中溶液 | 選用指示劑 | 選用滴定管 | |
| A | 堿 | 酸 | 石蕊 | (乙) |
| B | 酸 | 堿 | 甲基橙 | (甲) |
| C | 堿 | 酸 | 酚酞 | (甲) |
| D | 酸 | 堿 | 石蕊 | (乙) |
| 待測氫氧化鈉 | 0.100mol/L醋酸的體積 | ||
| 滴定次數 | 溶液的體積(mL) | 滴定前的刻度(mL) | 滴定后的刻度(mL) |
| 第一次 | 25.00 | 0.00 | 24.98 |
| 第二次 | 25.00 | 1.56 | 27.86 |
| 第三次 | 25.00 | 0.22 | 25.24 |
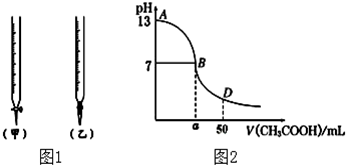
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com