
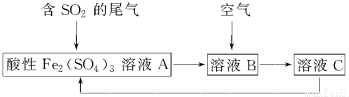
| A. | 溶液B中發生的反應為2SO2+O2═2SO3 | |
| B. | 可用酸性高錳酸鉀溶液檢驗溶液C中是否含有Fe3+ | |
| C. | 由以上流程可推知氧化性:Fe3+>O2>SO42- | |
| D. | 此工藝的優點之一是物質能循環利用 |
分析 依據處理二氧化硫氣體的工藝流程,各步反應都是完全反應,尾氣中的二氧化硫氣體,通入酸性硫酸鐵溶液中發生氧化還原反應,三價鐵離子氧化二氧化硫為硫酸,本身被還原為B溶液含有二價鐵離子,通入空氣會氧化亞鐵離子得到含三價鐵離子的溶液C,溶液C可以循環運用.
解答 解:A、溶液B中發生的反應是亞鐵離子被氧氣氧化為三價鐵離子的反應:4Fe2++O2+4H+=4Fe3++2H2O,故A錯誤;
B、酸性高錳酸鉀與鐵離子不能反應,故B錯誤;
C、由反應可知:2Fe3++2H2O+SO2=2Fe2++SO42-+4H+;4Fe2++O2+4H+=4Fe3++2H2O;依據氧化還原反應中氧化劑的氧化性大于氧化產物,所以氧化性O2>Fe3+>SO42-,故C錯誤;
D、過程中生成的硫酸鐵溶液可以循環使用,故D正確;
故選D.
點評 本題考查了污染氣體二氧化硫的回收利用工藝流程的分析判斷,氧化還原反應的規律應用,主要是考查二氧化硫的還原性、三價鐵離子的氧化性、二價鐵離子的還原性的性質應用,注意反應的產物判斷是本題的關鍵.


 七星圖書口算速算天天練系列答案
七星圖書口算速算天天練系列答案 初中學業考試導與練系列答案
初中學業考試導與練系列答案科目:高中化學 來源: 題型:選擇題
| A. | 該反應中熵變小于0、焓變大于0 | |
| B. | 判斷反應能否自發進行需要根據△H與△S綜合考慮 | |
| C. | 該反應是吸熱反應,因此一定不能自發進行 | |
| D. | 碳酸鹽分解反應中熵增加,因此任何條件下所有碳酸鹽分解一定自發進行 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
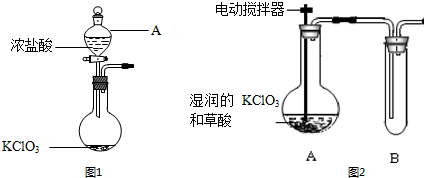

查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
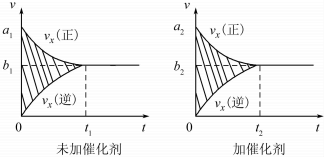
| 溫度/℃ | 800 | 1000 | 1200 | 1400 |
| 平衡常數 | 0.45 | 1.92 | 276.5 | 1771.5 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

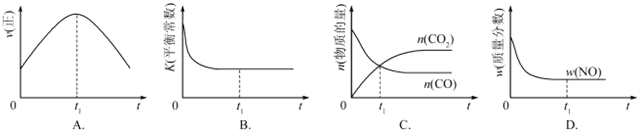
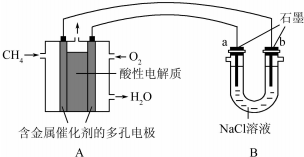
| A. | 圖①表示將SO2氣體通入溴水中溶液PH值隨SO2氣體變化關系 | |
| B. | 圖②表示反應N2(g)+3H2($?_{催化劑}^{高溫、高壓}$g)2NH3(g)△H<0的平衡常數K隨溫度的變化 | |
| C. | 圖③中陰、陽兩極收集到的氣體體積之比一定為1:1 | |
| D. | 圖④中的△H1<△H2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 當△H為“-”時,表示該反應為吸熱反應 | |
| B. | 化學反應的反應熱只與反應體系的始態和終態有關,而與反應的途徑無關 | |
| C. | H2S的燃燒熱△H=-a kJ•mol-1,則表示H2S燃燒熱的熱化學方程式為2H2S(g)+3O2(g)═2SO2(g)+2H2O(l)△H=-2a kJ•mol-1 | |
| D. | 反應熱的大小與反應物所具有的能量和生成物所具有的能量無關 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
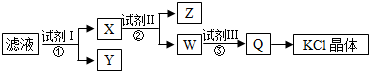
| A. | 圖示的步驟中必需要經過2次過濾操作 | |
| B. | 起始濾液呈中性 | |
| C. | 試劑Ⅱ為Na2CO3溶液 | |
| D. | 試劑Ⅲ為鹽酸 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com