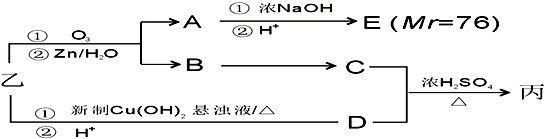
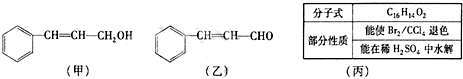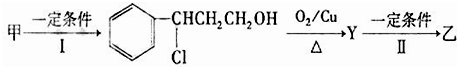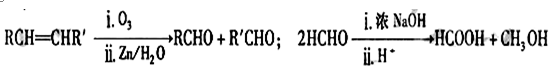固體硝酸鹽加熱易分解且產物較復雜.某學習小組以Mg(NO
3)
2為研究對象,擬通過實驗探究其熱分解的產物,提出如下4種猜想:
甲:Mg(NO
3)
2、NO
2、O
2 乙:MgO、NO
2、O
2 丙:Mg
3N
2、O
2 丁:MgO、NO
2、N
2(1)實驗前,小組成員經討論認定猜想丁不成立,理由是
.
查閱資料得知:2NO
2+2NaOH═NaNO
3+NaNO
2+H
2O,針對甲、乙、丙猜想,設計如圖所示的實驗裝置(圖中加熱、夾持儀器等均省略):

(2)實驗過程:
①取器連接后,放人固體試劑之前,關閉k,微熱硬質玻璃管(A),觀察到E 中有氣泡連續放出,表明
.
②稱取Mg(NO
3)
2固體3.79g置于A中,加熱前通入N
2以驅盡裝置內的空氣,其目的是避免對產物O
2的檢驗產生干擾;關閉K,用酒精燈加熱時,正確操作是先
然后固定在管中固體部位下加熱.
③觀察到A中有紅棕色氣體出現,C、D中未見明顯變化.
④待樣品完全分解,A裝置冷卻至室溫、稱量,測得剩余固體的質量為1.0g
⑤取少量剩余固體于試管中,加人適量水,未見明顯現象.
(3)實驗結果分析討論
①根據實驗現象和剩余固體的質量經分析可初步確認猜想
是正確的.
②根據D中無明顯現象,一位同學認為不能確認分解產物中有O
2,因為若有O
2,D中將發生氧化還原反應:
(填寫化學方程式),溶液顏色會退去;小組討論認定分解產物中有O
2存在,未檢側到的原因是O
2在通過裝置B時已參與反應.
③小組討論后達成的共識是上述實驗設計仍不完善,需改進裝置進一步研究.

 液態HCl
液態HCl NaOH固體
NaOH固體 液態HCl
液態HCl NaOH固體都是化合物,在水溶液或者熔融狀態下能夠導電屬于電解質;
NaOH固體都是化合物,在水溶液或者熔融狀態下能夠導電屬于電解質;
 ;②⑥⑩;
;②⑥⑩;