
| A. | 10gD2O中含有的電子數為5NA | |
| B. | 1molC3H8分子中共價鍵總數為10NA | |
| C. | 92gNO2和N2O4混合氣體中含有原子數為3NA | |
| D. | 65gZn全部溶解在一定濃度的硝酸溶液中,有NO生成,則轉移的電子數為2NA |
分析 A.D2O中含有10個電子,重水的摩爾質量為20g/mol,據此進行計算10g重水含有的電子數;
B.丙烷分子中含有2個碳碳鍵和8個碳氫鍵,總共含有10個共價鍵;
C.NO2和N2O4最簡式同為NO2,根據最簡式計算92gNO2中所含原子數;
D.鋅為2價金屬,65g鋅的物質的量為1mol,完全反應轉移2mol電子.
解答 解:A.10g重水(D2O)的物質的量是:$\frac{10g}{20g/mol}$=0.5mol,D2O分子中含有10個電子,則0.5mol重水中含有的電子數為5NA,故A正確;
B.1molC3H8分子中含有2mol碳碳鍵、8mol碳氫鍵,總共含有10mol共價鍵,含有的共價鍵總數為10NA,故B正確;
C.92gNO2和N2O4的混合物中含有最簡式NO2的物質的量為:$\frac{92g}{46g/mol}$=2mol,則混合物中含有的原子數=2×3×NA=6NA,故C錯誤;
D.65gZn的物質的量為1mol,1mol鋅全部溶解在一定濃度的硝酸溶液中,最多失去2mol電子,則轉移的電子數為2NA,故D正確;
故選C.
點評 本題考查了阿伏伽德羅常數的綜合應用,題目難度中等,掌握好以物質的量為中心的各化學量與阿伏加德羅常數的關系為解答關鍵,C為易錯點,注意明確最簡式在化學計算中的應用.


科目:高中化學 來源: 題型:選擇題
| A. | 常溫下,28g C2H4中含有的極性共價鍵數為6NA | |
| B. | 在氫氧化鋇溶液中加入少量的硫酸氫鈉溶液:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O | |
| C. | 濃度均為0.1 mol•L-1的C6H5ONa溶液和CH3COONa溶液中:陰離子的總濃度前者小于后者 | |
| D. | 常溫下,濃度分別為0.1 mol•L-1和0.01 mol•L-1的CH3COOH溶液中:CH3COO-離子濃度前者是后者的10倍 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①② | B. | ①④ | C. | ②③ | D. | ③④ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,22.4 L HCl溶于水后溶液中含有nA個HCl分子 | |
| B. | 1L 0.1 mol•L-1的Na2SO4溶液中含有0.2 nA個Na+ | |
| C. | 1 mol 硫酸鉀中陰離子所帶電荷數為nA | |
| D. | 將0.1mol氯化鐵溶于1L水中,所得溶液含有0.1nAFe3+ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 3:1 | B. | 3:2 | C. | 2:1 | D. | 1:2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
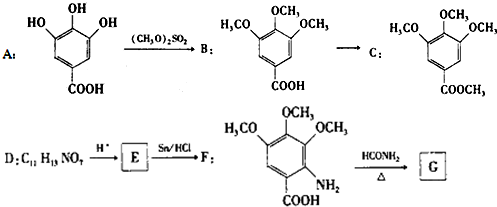
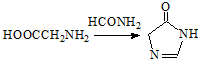
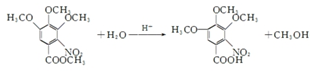 .
.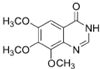 .
.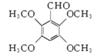 .
.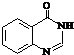 .合成過程中無機試劑任選.
.合成過程中無機試劑任選.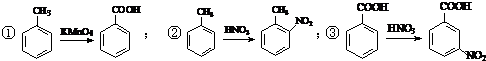 )
)查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 增加SO2的濃度 | B. | 充入一定量惰性氣體 | ||
| C. | 升高溫度 | D. | 使用催化劑 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
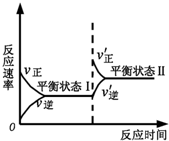
| A. | 反應達平衡時,正反應速率和逆反應速率相等 | |
| B. | 該反應達到平衡狀態Ⅰ后,減小反應物濃度,平衡發生移動,達到平衡狀態Ⅱ | |
| C. | 該反應達到平衡狀態Ⅰ后,增大反應物濃度,平衡發生移動,達到平衡狀態Ⅱ | |
| D. | 同一種反應物在平衡狀態Ⅰ和平衡狀態Ⅱ時濃度不相等 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com