
| A. | 常溫下,28g C2H4中含有的極性共價鍵數為6NA | |
| B. | 在氫氧化鋇溶液中加入少量的硫酸氫鈉溶液:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O | |
| C. | 濃度均為0.1 mol•L-1的C6H5ONa溶液和CH3COONa溶液中:陰離子的總濃度前者小于后者 | |
| D. | 常溫下,濃度分別為0.1 mol•L-1和0.01 mol•L-1的CH3COOH溶液中:CH3COO-離子濃度前者是后者的10倍 |
分析 A、乙烯的相對分子質量為28,根據乙烯的結構計算,結構為: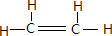 ;
;
B、少量硫酸氫鈉溶液與氫氧化鋇溶液反應,硫酸氫鈉完全反應,生成硫酸鋇、水、NaOH;
C、C6H5ONa的水解程度大于CH3COONa,結合電荷守恒分析;
D、醋酸是弱酸,醋酸溶液的濃度越小電離程度越大.
解答 解:A、28g乙烯的物質的量為$\frac{28g}{28g/mol}$=1mol,根據乙烯的結構: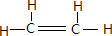 ,可知1mol乙烯中含有4mol極性共價鍵,極性共價鍵數目為4NA,故A錯誤;
,可知1mol乙烯中含有4mol極性共價鍵,極性共價鍵數目為4NA,故A錯誤;
B、少量硫酸氫鈉溶液滴到氫氧化鋇溶液中,硫酸氫鈉完全反應,生成硫酸鋇、水、NaOH,離子反應為Ba2++OH-+H++SO42-═BaSO4↓+H2O,故B錯誤;
C、C6H5ONa溶液中電荷守恒為c(C6H5O-)+c(OH-)=c(Na+)+c(H+),CH3COONa溶液中電荷守恒為c(CH3COO-)+c(OH-)=c(Na+)+c(H+),C6H5ONa的水解程度大于CH3COONa,則C6H5ONa溶液中堿性強,所以C6H5ONa中c(H+)小,已知兩個溶液中c(Na+)相同,所以C6H5ONa中c(Na+)+c(H+)小于CH3COONa溶液,因此
濃度均為0.1 mol•L-1的C6H5ONa溶液和CH3COONa溶液中:陰離子的總濃度前者小于后者,故C正確;
D、醋酸溶液的濃度越小電離程度越大,因此0.1 mol/L的CH3COOH溶液與0.01 mol/L的CH3COOH溶液中:CH3COO-離子濃度前者小于后者濃度的10倍,故D錯誤.
故選C.
點評 本題主要考查了弱電解質的電離、鹽的水解原理及應用,明確弱電解質電離平衡特點和影響因素,以及鹽的水解原理是解本題關鍵,題目難度中等.


 小學生10分鐘口算測試100分系列答案
小學生10分鐘口算測試100分系列答案科目:高中化學 來源: 題型:解答題
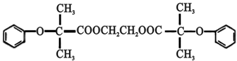 )可由下列路線合成:
)可由下列路線合成: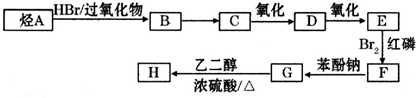
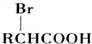
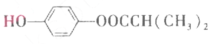 .
.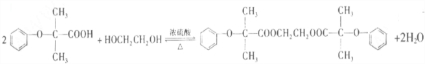 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 乙烯通入溴的四氯化碳溶液中,溶液褪色 | |
| B. | 苯滴加到溴水中,振蕩后水層接近無色 | |
| C. | 將灼熱的銅絲迅速插入乙醇中,反復多次,有刺激性氣味產生 | |
| D. | 甲烷和氯氣的混合氣體在光照后,瓶壁上有油狀液滴附著 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
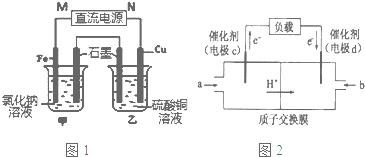
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在1 mol CaC2、KHSO4、KO2(超氧化鉀)三種離子化合物中,所含陰、陽離子的總數均為3NA | |
| B. | 0.1 mol C2H2OH中所含C-H鍵的數目為0.6NA | |
| C. | S2和S8的混合物共6.4g,其中所含硫原子數一定為0.2NA | |
| D. | 78gNa2O2與足量水反應轉移的電子數為2NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 除去溶液中Ag+加鹽酸鹽比硫酸鹽好 | |
| B. | 加入H20,溶解平衡不移動 | |
| C. | 用NaCl溶液代替蒸餾水洗滌AgCl,可以減少沉淀損失 | |
| D. | 反應2AgCl+Na2S═Ag2S+2NaCl 說明溶解度:AgCl>Ag2S |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
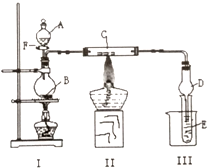 用如圖所示裝置進行有關實驗,拔掉分液漏斗上口玻璃塞,打開F,將A逐滴加入至B中.
用如圖所示裝置進行有關實驗,拔掉分液漏斗上口玻璃塞,打開F,將A逐滴加入至B中.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 10gD2O中含有的電子數為5NA | |
| B. | 1molC3H8分子中共價鍵總數為10NA | |
| C. | 92gNO2和N2O4混合氣體中含有原子數為3NA | |
| D. | 65gZn全部溶解在一定濃度的硝酸溶液中,有NO生成,則轉移的電子數為2NA |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com