
 某同學設計了如圖所示的裝置,可比較HNO3、H2CO3、H2SiO3的酸性強弱,進而比較氮、碳、硅元素非金屬性強弱.供選擇的試劑:稀硝酸、稀硫酸、碳酸鈣固體、碳酸鈉固體、硅酸鈉溶液、澄清石灰水、飽和碳酸氫鈉溶液
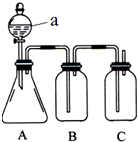
某同學設計了如圖所示的裝置,可比較HNO3、H2CO3、H2SiO3的酸性強弱,進而比較氮、碳、硅元素非金屬性強弱.供選擇的試劑:稀硝酸、稀硫酸、碳酸鈣固體、碳酸鈉固體、硅酸鈉溶液、澄清石灰水、飽和碳酸氫鈉溶液分析 比較HNO3、H2CO3、H2SiO3的酸性強弱,由實驗裝置可知,a為分液漏斗,a為硝酸,在A中硝酸與碳酸鈉發生強酸制取弱酸的反應,B中為碳酸氫鈉溶液除去揮發的硝酸,在C中二氧化碳與硅酸鈉發生強酸制取弱酸的反應,以此可比較酸性,最高價氧化物的水化物酸性越強,則對應非金屬的非金屬性越強,以此來解答.
解答 解:由實驗裝置可知,a為分液漏斗,a為硝酸,在A中硝酸與碳酸鈉發生強酸制取弱酸的反應,B中為碳酸氫鈉溶液除去揮發的硝酸,在C中二氧化碳與硅酸鈉發生強酸制取弱酸的反應,
(1)由圖可知,a為分液漏斗,故答案為:分液漏斗;
(2)由上述分析可知,a中試劑為稀硝酸,故答案為:稀硝酸;
(3)B的作用為吸收氣體中硝酸,且不能吸收二氧化碳,則B中試劑為飽和碳酸氫鈉溶液,故答案為:飽和碳酸氫鈉溶液;吸收氣體中硝酸;
(4)C中試劑為硅酸鈉溶液,發生離子反應為SiO32-+CO2+H2O=H2SiO3↓+CO32-,故答案為:;SiO32-+CO2+H2O=H2SiO3↓+CO32-;
(5)由上述實驗可知,酸性為硝酸>碳酸>硅酸,則非金屬性N>C>Si,故答案為:N>C>Si.
點評 本題考查酸性及非金屬性比較的探究實驗,為高頻考點,注意硝酸有揮發性,導致二氧化碳氣體中含有硝酸會對實驗造成干擾,側重分析與實驗能力的綜合考查,題目難度不大.


科目:高中化學 來源: 題型:選擇題
| A. | 離子半徑:Al3+>Mg2+>F- | B. | 熱穩定性:HI>HBr>HCl>HF | ||
| C. | 酸性:H2SiO3<H3PO4<H2SO4<HClO4 | D. | 堿性:Al(OH)3>Mg(OH)2>NaOH |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 容器內氣體混合物的密度不隨時間變化 | |
| B. | 容器內X、Y、Z的濃度之比為1:2:2 | |
| C. | 單位時間內消耗0.1mol X,同時生成0.2mol Y | |
| D. | 單位時間內消耗0.1mol X,同時生成0.2mol Z |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 敘述I | 敘述II |
| A | 苯甲酸的溶解度隨溫度升高而增大 | 用蒸發濃縮、冷卻結晶、過濾,除去苯甲酸中混有的泥沙 |
| B | NH4Cl受熱容易分解 | 加熱NH4Cl制備NH3 |
| C | SO2具有漂白性 | SO2能使酸性KMnO4溶液褪色 |
| D | 某溫度下,碳酸的K1=4.4×10-7,次氯酸的K=2.98×10-8 | 用CO2和NaClO溶液制備HClO |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 物質的量相等的185Hf與180Hf質量相同 | |
| B. | 核外電子數分別為108、113 | |
| C. | 1 mol 180Hf比1 mol 185Hf的中子數少5NA | |
| D. | 180Hf、185Hf在周期表中的位置不同 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ③①②④ | B. | ④①②③ | C. | ①②③④ | D. | ④③②① |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com