
| ||
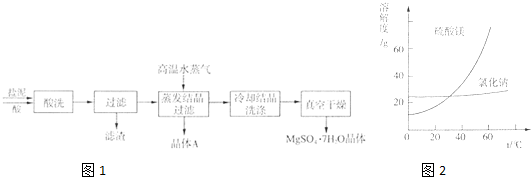
| 成分 | NaCl | Mg(OH)2 | CaCO3 | BaSO4 | 其他不溶物 |
| 質量分數(%) | 15~20 | 15~20 | 5~10 | 30~40 | 10~15 |
| 1371g |
| x |
| 100g+37.1g |
| 37.1g |
| 117 |
| 351 |
| 80 |
| m |
| 1152g |
| 1.37g?cm -3 |
| 1371g |
| x |
| 100g+37.1g |
| 37.1g |
| 117 |
| 351 |
| 80 |
| m |
| 1152g |
| 1.37g?cm -3 |
| n |
| V |


科目:高中化學 來源: 題型:

查看答案和解析>>
科目:高中化學 來源: 題型:
| ①CH3COOH | ②H2CO3 | ③H2S | ④H4PO4 |
| 1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=9.1×10-8 K2=1.1×10-12 | K1=7.5×10-3 K2=6.2×10-8 K3=2.2×10-13 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、①②④⑤ | B、③⑥ |
| C、②④⑤ | D、②④⑥ |
查看答案和解析>>
科目:高中化學 來源: 題型:
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ⑦ | ? | ||||||
| 三 | ① | ③ | ⑤ | ⑥ | ⑧ | ⑩ | ||
| 四 | ② | ④ | ⑨ |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、0.01mol?L-1醋酸溶液 |
| B、0.02mol?L-1醋酸與0.01mol?L-1NaOH溶液等體積混合液 |
| C、0.03mol?L-1醋酸與0.01mol?L-1NaOH溶液等體積混合液 |
| D、pH=2的鹽酸與0.01mol?L-1NaOH溶液等體積混合液 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、0.01 mol?L-1 |
| B、0.02 mol?L-1 |
| C、1×10-12 mol?L-1 |
| D、5×10-13 mol?L-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:
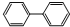 ,下列有關聯苯的說法中正確的是( )
,下列有關聯苯的說法中正確的是( )| A、分子中含有6個碳碳雙鍵 |
| B、聯苯的一硝基取代產物的3種 |
| C、它容易發生加成反應、取代反應,容易被強氧化劑氧化 |
D、它和蒽(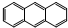 )同屬于芳香烴,兩者互為同系物 )同屬于芳香烴,兩者互為同系物 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、原子半徑:A<B<C |
| B、C的最簡單氫化物的穩定性大于A的最簡單氫化物的穩定性 |
| C、高溫下,A單質能置換出C單質 |
| D、三種元素的最高價氧化物對應的水化物均可由化合反應得到 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com