
| A. | 氯氣溶于水:Cl2+H2O═2H++Cl-+ClO- | |
| B. | 飽和Na2CO3溶液中通入足量CO2:2Na++CO32-+CO2+H2O═2NaHCO3↓ | |
| C. | 酸性溶液中KIO3與KI反應生成I2:IO3-+5I-+6H+═3I2+3H2O | |
| D. | 漂白粉溶液中加入醋酸:CH3COOH+ClO-═HClO+CH3COO- |
分析 A.次氯酸為弱酸,應保留化學式;
B.飽和Na2CO3溶液中通入足量CO2生成碳酸氫鈉晶體;
C.碘酸鉀與碘化鉀在酸性環境下反應生成碘和水;
D.二者反應生成次氯酸和醋酸鈣.
解答 解:A.氯氣溶于水,離子方程式:Cl2+H2O═H++Cl-+HClO,故A錯誤;
B.飽和Na2CO3溶液中通入足量CO2,離子方程式:2Na++CO32-+CO2+H2O═2NaHCO3↓,故B正確;
C.酸性溶液中KIO3與KI反應生成I2,離子方程式:IO3-+5I-+6H+═3I2+3H2O,故C正確;
D.漂白粉溶液中加入醋酸,離子方程式:CH3COOH+ClO-═HClO+CH3COO-,故D正確;
故選:A.
點評 本題考查了離子方程式的書寫,明確反應實質及離子方程式書寫方法是解題關鍵,注意化學式的拆分,題目難度不大.


科目:高中化學 來源: 題型:選擇題
| A. | 質子數 | B. | 質量數 | C. | 中子數 | D. | 電子數 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題

| A. | Fe2+、I-、Cl-三種離子一定存在 | |
| B. | 不能確定Na+和Cl-是否存在,CO${\;}_{3}^{2-}$一定不存在 | |
| C. | Fe3+與Fe2+至少有一種 | |
| D. | 該溶液中c(Cl-)≥0.1mol•L-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 加入水時,平衡向右移動,CH3COOH電離常數增大 | |
| B. | 加入少量CH3COONa固體,平衡向右移動 | |
| C. | 加入少量NaOH固體,平衡向右移動,c(H+)減小 | |
| D. | 加入少量pH=5的硫酸,溶液中c(H+)增大 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 玻璃鋼和鋼化玻璃成分不同,但都屬于復合材料 | |
| B. | Fe(OH)3膠體無色、透明,能發生丁達爾現象 | |
| C. | H2、SO2、Cl2都可用濃硫酸干燥 | |
| D. | SiO2既能和NaOH溶液反應又能和氫氟酸反應,所以是兩性氧化物 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
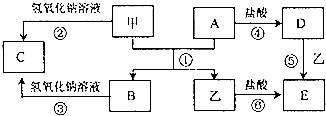
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| ① | ② | ③ | ||
| ④ | ⑤ | ⑥ | ⑦ |
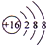 、
、 ,這兩種離子的半徑大小順序是S2->Cl-(填化學式).
,這兩種離子的半徑大小順序是S2->Cl-(填化學式).查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 溫度/℃ | 1000 | 1115 | 1300 |
| 平衡常數 | 4.0 | 3.7 | 3.5 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 某氣體$\stackrel{通入品紅溶液中}{→}$品紅溶液褪色 結論:某氣體一定是SO2 | |
| B. | 某氣體$\stackrel{通入澄清石灰水}{→}$ 產生白色沉淀 結論:某氣體一定是CO2 | |
| C. | 某溶液$\stackrel{打開瓶蓋}{→}$冒白霧$\stackrel{將沾有濃氨水的玻璃棒靠近}{→}$ 白煙 結論:原溶液一定是濃鹽酸 | |
| D. | 某溶液$\stackrel{滴加KSCN溶液液}{→}$ 血紅色溶液 結論:原溶液中一定含有Fe3+ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com