
 某同學設計出如下裝置成功的證明了Cu和Ag的金屬活動性順序.請你原電池原理和實驗裝置,完成下列實驗報告.
某同學設計出如下裝置成功的證明了Cu和Ag的金屬活動性順序.請你原電池原理和實驗裝置,完成下列實驗報告.分析 利用置換反應Cu+2AgNO3=Cu(NO3)2+2Ag,說明Cu和Ag的金屬活動性順序,據此設計原電池時,Cu為負極,Ag為正極,工作時,正極反應式為Ag++e-=Ag,有金屬析出,負極反應式為Cu-2e-=Cu2+,Cu逐漸溶解,根據原電池的工作原理來回答即可.
解答 解:(1)原電池時,Cu為負極,Ag為正極,電解質是硝酸銀溶液,故答案為:銀片;銅片;參與氧化還原反應和導電;
(2)原電池的正極上是電解質中的陽離子得電子的還原反應,即Ag++e-=Ag,負極上是電極本身發生失電子的氧化反應,即Cu-2e-=Cu2+,
故答案為:Ag++e-=Ag;Cu-2e-=Cu2+;
(3)負極上是電極本身發生失電子的氧化反應,電極不斷溶解,正極上是電解質中的陽離子銀離子得電子的還原反應,有白色的銀單質析出,溶液從無色變為藍色,故答案為:負極不斷溶解,正極上有白色的銀單質析出,溶液從無色變為藍色;
(4)根據原電池反應的現象,得出金屬Cu可以將金屬銀從其鹽中置換出來,所以金屬的活潑性是Cu>Ag,故答案為:金屬的活潑性是Cu>Ag;
點評 本題考查學生原電池的工作原理、應用以及電極反應式的書寫等方面的知識,屬于綜合知識的考查,難度中等.


科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ②③④⑥ | B. | ①②⑥ | C. | ②③④⑤ | D. | ①③⑤ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
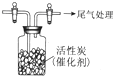 某學習小組推測SO2能與強氧化劑Cl2反應生成SO2Cl2,為此進行探究.
某學習小組推測SO2能與強氧化劑Cl2反應生成SO2Cl2,為此進行探究.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 還原性X-強于Y2- | |
| B. | X的含氧酸的酸性比Y的含氧酸的酸性強 | |
| C. | X的單質X2能將Y的陰離子Y2-氧化,并發生置換反應 | |
| D. | X的氫化物比Y的氫化物沸點高 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
 反應:L(s)+aG(g)?bR(g) 達到平衡時,溫度和壓強對該反應的影響如圖所示:圖中壓強p1>p2,x軸表示溫度,y軸表示平衡混合氣中G的體積分數.
反應:L(s)+aG(g)?bR(g) 達到平衡時,溫度和壓強對該反應的影響如圖所示:圖中壓強p1>p2,x軸表示溫度,y軸表示平衡混合氣中G的體積分數.| A. | a<b | B. | 上述反應是吸熱反應 | ||
| C. | a>b | D. | 上述反應是放熱反應 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com