
| A. | 向某溶液中加入BaCl2溶液,產生白色沉淀,再加鹽酸,沉淀不溶解,該溶液一定含有SO42- | |
| B. | 向某溶液中同時加入幾滴KSCN溶液和少量新制氯水,溶液變為紅色,該溶液一定含有Fe2+ | |
| C. | 向某溶液中加入稀鹽酸,產生能使澄清石灰水變渾濁的無色氣體,該溶液不一定含有CO32- | |
| D. | 向某溶液中加入稀硝酸后,再加入AgNO3溶液,產生白色沉淀,則該溶液中含有Cl- |
分析 A.白色沉淀可能為AgCl或硫酸鋇;
B.加入幾滴KSCN溶液和少量新制氯水,可能原溶液含鐵離子,或亞鐵離子被氧化生成鐵離子;
C.無色氣體為二氧化碳或二氧化硫;
D.白色沉淀為AgCl.
解答 解:A.白色沉淀可能為AgCl或硫酸鋇,則該溶液可能含有SO42-或銀離子,但二者不能同時存在,故A錯誤;
B.加入幾滴KSCN溶液和少量新制氯水,可能原溶液含鐵離子,或亞鐵離子被氧化生成鐵離子,檢驗亞鐵離子應先加KSCN溶液無現象,再加氯水為血紅色,故B錯誤;
C.無色氣體為二氧化碳或二氧化硫,則溶液不一定含有CO32-,故C正確;
D.硝酸可排除干擾離子,白色沉淀為AgCl,則該溶液中含有Cl-,故D正確;
故選CD.
點評 本題考查常見離子的檢驗,為高頻考點,把握離子檢驗的試劑、現象、結論為解答的關鍵,側重分析與實驗能力的考查,注意排除干擾離子的影響,題目難度不大.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:多選題
| A. | 反應一段時間后,X與Y的物質的量之比仍為1:1 | |
| B. | 達到平衡時,且反應放出0.1aKJ的熱量 | |
| C. | 達到平衡后,若向平衡體系中充入稀有氣體,Z的正反應速率將不發生變化 | |
| D. | X的體積分數保持不變,說明反應已達到平衡 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 應用 | 解釋 |
| A | 在相同條件下,在兩支試管中各加入2mL 5% H2O2溶液,再向H2O2溶液中分別滴入1mL H2O和1mL 0.1mol•L-1 FeCl3溶液,對比觀察現象 | 可以探究催化劑FeCl3對H2O2 分解速率的影響 |
| B | 向盛有1mL 0.01mol•L-1 AgNO3溶液的試管中滴加5滴0.01mol•L-1 NaCl溶液,有白色沉淀生成,再向其中滴加0.01mol•L-1 KI溶液,產生黃色沉淀. | 常溫下,Ksp(AgCl)>Ksp(AgI) |
| C | 向兩份蛋白質溶液中分別滴加飽和NaCl溶液和CuSO4溶液,均有固體析出 | 蛋白質均發生變性 |
| D | 保存硫酸亞鐵溶液需加入少量稀鹽酸和鐵釘 | 防止 Fe2+水解以及被 O2 氧化 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | NaOH | B. | NH3•H2O | C. | CuO | D. | Cu(OH)2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 大氣中大量的NO、NO2等酸性氧化物均是形成酸雨(PH>5.6)的主要原因 | |
| B. | 合成纖維,光導纖維,硝酸纖維均為有機高分子物質,用途廣泛 | |
| C. | 二氧化硫和氯水均具有漂白性,可將兩者混合使用增強漂白效果 | |
| D. | 地溝油,潲水油在餐飲企業中不能隨意使用,但卻可以用于制肥皂,變廢為寶 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.4 mol | B. | 0.34 mol | C. | 0.8 mol | D. | 0.74 mol |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.1mol•L-1的HF溶液加水稀釋過程中,HF的電離平衡常數逐漸增大 | |
| B. | pH=12的NaOH溶液與pH=2的醋酸溶液等體積混合后,溶液呈中性 | |
| C. | pH=5的NaHSO3溶液中水電離出的H+濃度小于10-71mol•L-1 | |
| D. | 向Na2CO3,Na2SO4的混合溶液中逐滴加入BaCl2溶液,一定先生成BaSO4 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
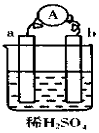
| A. | 碳棒上有氣體放出,溶液pH變大 | |
| B. | a是正極,b是負極 | |
| C. | 導線中有電子流動,外電路中,電流從b極到a極 | |
| D. | a極上發生了氧化反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
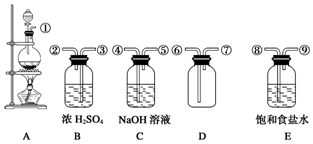
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com