
| A. | 1mol[Cu(NH3)4]SO4•H2O分解產生氣體體積為97.1L | |
| B. | 生成1molCu轉移2mol電子 | |
| C. | 分解產生的氣體通入BaCl2溶液有白色沉淀生成 | |
| D. | 可以用濕潤的紅色石蕊試紙直接檢驗此反應產生的氨氣 |
分析 A、狀況不知無法求體積;
B、由反應可知:3[Cu(NH3)4]SO4•H2O$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+8NH3↑+2N2↑+3SO2↑+9H2O,氮由-3價變成0價,轉移電子為12mol;
C、氨氣溶于水生成一水合氨,一水合氨電離產生氫氧根離子,溶液顯堿性,通入二氧化硫反應生成亞硫酸銨,亞硫酸銨與氯化鋇反應生成亞硫酸鋇沉淀;
D、分解產生的氣體中有二氧化硫氣體,所以應首先用堿溶液吸收二氧化硫,然后再將所得氣體通入濕潤的紅色石蕊試紙觀察現象.
解答 解:A、狀況不知無法求體積,故A錯誤;
B、由反應可知:3[Cu(NH3)4]SO4•H2O$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+8NH3↑+2N2↑+3SO2↑+9H2O,氮由-3價變成0價,轉移電子為12mol,所以生成1molCu轉移4mol電子,故B錯誤;
C、氨氣溶于水生成一水合氨,一水合氨電離產生氫氧根離子,溶液顯堿性,通入二氧化硫反應生成亞硫酸銨,亞硫酸銨與氯化鋇反應生成亞硫酸鋇沉淀,故C正確;D、分解產生的氣體中有二氧化硫氣體,所以應首先用堿溶液吸收二氧化硫,然后再將所得氣體通入濕潤的紅色石蕊試紙觀察現象,故D錯誤;
故選C.
點評 本題考查了氧化還原反應的相關知識,熟悉氨氣的檢驗方法是解題關鍵,題目難度不大,注重基礎知識夯實.


科目:高中化學 來源: 題型:選擇題
| A. | Fe+Cu2+═Fe2++Cu | |
| B. | Cl2+H2O═HCl+HClO | |
| C. | 2CH3COOH+Ca(ClO)2═2HClO+Ca(CH3COO)2 | |
| D. | 4HCl+MnO2═MnCl2+Cl2↑+H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 向盛有50mL 1.00mol•L-1 HCl溶液的絕熱容器中加入NaOH溶液,NaOH溶液的體積(V)與所得混合溶液的最高測量溫度(T)的關系如圖所示,下列敘述中不正確的是( )
向盛有50mL 1.00mol•L-1 HCl溶液的絕熱容器中加入NaOH溶液,NaOH溶液的體積(V)與所得混合溶液的最高測量溫度(T)的關系如圖所示,下列敘述中不正確的是( )| A. | 該實驗表明化學能可以轉化為熱能 | |
| B. | NaOH溶液的濃度大于1.00 mol•L-1 | |
| C. | V=50 mL時,混合液呈堿性 | |
| D. | 該實驗表明有水生成的反應都是放熱反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 ⑦
⑦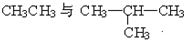
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 同一周期元素的原子,半徑越小越容易失去電子 | |
| B. | ⅠA族元素的金屬性比ⅡA族元素的金屬性強 | |
| C. | 若M+和R2-的核外電子層結構相同,則原子序數:R<M | |
| D. | 主族元素的最高正化合價等于該元素原子的核外電子數 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 金屬Na、Mg、A1熔、沸點由高到低 | |
| B. | HC1、HBr、HI的還原性由弱到強 | |
| C. | H+、Li+、H-的半徑由小到大 | |
| D. | 同濃度的硫酸鈉、乙酸鈉、碳酸鈉溶液的堿性由強到弱 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 反應開始時速率:甲=乙 | B. | 反應所需時間:乙>甲 | ||
| C. | 參加反應時鋅的質量:甲=乙 | D. | 兩份酸溶液物質的量濃度:乙>甲 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 上述反應屬于取代反應 | |
| B. | 對三聯苯的一氯取代物有3種 | |
| C. | 1 mol對三聯苯在足量的氧氣中完全燃燒消耗21.5 mol O2 | |
| D. | 對三聯苯分子中至少有16個原子共平面 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com