
| A. | 升高溫度,正反應速率增大,化學平衡常數增大 | |
| B. | 減小壓強,逆反應速率減小,化學平衡常數減小 | |
| C. | 加入催化劑,正逆反應速率不變,平衡不移動 | |
| D. | 充入氧氣,正反應速率先增大后減小,平衡向正反應方向移動 |
分析 A.升溫反應速率增大,正逆反應速率增大,反應是放熱反應,升溫平衡逆向進行;
B.減小壓強反應速率減小,平衡常數隨溫度變化,不隨壓強變化;
C.催化劑同等程度改變反應速率,但不改變化學平衡;
D.充入氧氣增大反應物的濃度,平衡正向進行,隨濃度減小正反應速率減小,逆反應速率增大最后達到相同;
解答 解:A.升溫反應速率增大,正逆反應速率增大,反應是放熱反應,升溫平衡逆向進行,平衡常數減小,故A錯誤;
B.減小壓強反應速率減小,平衡常數隨溫度變化,不隨壓強變化,減壓平衡常數不變,故B錯誤;
C.催化劑同等程度改變反應速率,但不改變化學平衡,速率改變,平衡不變,故C錯誤;
D.充入氧氣瞬間增大反應物的濃度,平衡正向進行,隨濃度減小正反應速率減小,逆反應速率增大最后達到相同,達到平衡狀態,故D正確;
故選D.
點評 本題考查了化學平衡、反應速率、平衡常數影響因素,注意反應特征分析,題目較簡單.


科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1:2 | B. | 2:3 | C. | 3:2 | D. | 1:1 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | KClO3在反應中得到電子 | |
| B. | ClO2是還原產物 | |
| C. | H2C2O4在反應中被還原 | |
| D. | 1mol H2C2O4參加反應有2mol電子轉移 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 只有②③ | B. | 只有③④ | C. | 都正確 | D. | 都錯誤 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 地溝油和礦物油都屬于酯類物質 | |
| B. | 人們用明礬對水進行消毒、殺菌 | |
| C. | 反應 原子利用率最高 原子利用率最高 | |
| D. | 甲烷、苯和油脂均不能使酸性KMnO4溶液褪色 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | a c f h | B. | a c e g | C. | a c e f h | D. | b d e h |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
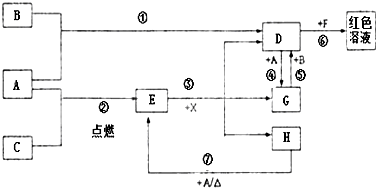 A、B、C為中學常見單質,其中一種為金屬;通常情況下A為固體、B為黃綠色氣體、C為無色氣體.D、E、F、G、H、X均為化合物,其中X常溫下是無色氣體,其水溶液是一種無氧強酸溶液,E為黑色固體,H在常溫下為液體.它們之間的轉化如圖所示(某些反應條件和部分反應產物已略去).
A、B、C為中學常見單質,其中一種為金屬;通常情況下A為固體、B為黃綠色氣體、C為無色氣體.D、E、F、G、H、X均為化合物,其中X常溫下是無色氣體,其水溶液是一種無氧強酸溶液,E為黑色固體,H在常溫下為液體.它們之間的轉化如圖所示(某些反應條件和部分反應產物已略去).查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com