
| 溫度(℃) | 10 | 20 | 30 | 加熱煮沸后冷卻到50℃ |
| pH | 8.3 | 8.4 | 8.5 | 8.8 |
分析 (1)NaHCO3為強堿弱酸鹽,在溶液中發生:HCO3-+H2O?H2CO3+OH-,水解呈堿性,加熱時,NaHCO3可分解生成Na2CO3,Na2CO3水解程度較大,溶液堿性較強;
(2)加入氯化鋇溶液后,如生成沉淀,說明乙同學結論正確;
(3)常壓下加熱NaHCO3的水溶液,溶液的溫度達不到150℃.
解答 解:(1)NaHCO3為強堿弱酸鹽,在溶液中發生:HCO3-+H2O?H2CO3+OH-,水解呈堿性,加熱時,NaHCO3可分解生成Na2CO3,Na2CO3水解程度較大,溶液堿性較強,
故答案為:HCO3-+H2O?H2CO3+OH-;大于;
(1)加入氯化鋇溶液后,如生成沉淀,說明溶液中存在大量的CO32-,乙同學結論正確,而加入A、D都生成沉淀不正確,加入C無現象,選試劑B,
故答案為:乙;B;
(2)如NaHCO3的分解溫度為150℃,則乙的結論肯定錯誤,原因是常壓下加熱NaHCO3的水溶液,溶液的溫度達不到150℃,
故答案為:乙;常壓下加熱NaHCO3的水溶液,溶液的溫度達不到150℃.
點評 本題考查較為綜合,涉及鹽類的水解和實驗方案的評價,側重于學生的實驗能力和評價能力的考查,注意把握鹽類水解的原理和規律,把握物質的性質,難度中等.


科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| 弱酸 | HCOOH | HCN | H2CO3 |
| 電離平衡常數 (25°C)) | Ki=1.77×10-4 | Ki=4.9×10-18 | Ki1=4.3×10-7 Ki2=5.6×10-11 |
| A. | CN-+H2O+CO2→HCN+HCO3- | |
| B. | 2HCOOH+CO32-→2HCOO-+H2O+CO2↑ | |
| C. | 中和等體積、等pH的HCOOH和HCN消耗NaOH的量前者大于后者 | |
| D. | 等體積、等濃度的HCOONa和NaCN溶液中所含離子總數前者小于后者 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1 mol Cl2與足量Fe反應,轉移的電子數為3NA | |
| B. | 3mol NO2與足量H2O反應,轉移的電子數為NA | |
| C. | 0.1mol/L的氫氧化鈉溶液中含鈉離子數為0.1NA個 | |
| D. | 0.30mol Fe粉與足量水蒸氣反應生成的H2分子數為0.40NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 物質 | 雜質 | 試劑 | 主要操作 | |
| A | SiO2 | Fe2O3 | 鹽酸 | 過濾 |
| B | Mg | Al | NaOH | 過濾 |
| C | FeCl2 | FeCl3 | Cu | 過濾 |
| D | KNO3 | KCl | H2O | 冷卻結晶 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 17g NH3和18 g H2O中含有的電子數均為10NA | |
| B. | 2 L 1.5 mol•L-1醋酸溶液中含有的CH3COO-數為3NA | |
| C. | 標準狀況下,5.6 L Cl2溶解于足量NaOH溶液中,轉移的電子數為0.5NA | |
| D. | 恒壓密閉容器中充入2 mol NO與1 mol NO2,容器中分子數為3NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氫氣在氯氣中安靜燃燒,發出蒼白色火焰 | |
| B. | 鐵絲在氯氣中燃燒,產生棕褐色的煙 | |
| C. | 銅絲在氯氣中燃燒,產生棕黃色的煙 | |
| D. | 鈉在氯氣中燃燒,產生黃色的煙 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
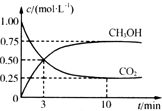 二氧化碳是地球溫室效應的罪魁禍首,目前人們處理二氧化碳的方法之一是使其與氫氣反應合成甲醇.已知氫氣、甲醇燃燒的熱化學方程式如下:
二氧化碳是地球溫室效應的罪魁禍首,目前人們處理二氧化碳的方法之一是使其與氫氣反應合成甲醇.已知氫氣、甲醇燃燒的熱化學方程式如下:| 物質 | CH3OH | CH3OCH3 | H2O |
| 濃度/(mol/L) | 0.44 | 0.6 | 0.6 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①⑥ | B. | ①②③④⑥ | C. | ①②③⑥ | D. | ①②③④ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com