
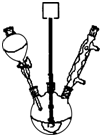
 如圖所示,隔板Ⅰ固定不動,活塞Ⅱ可自由移動,M、N兩個容器中均發生反應:A(g)+3B(g)?2C(g)△H=-192kJ?mol-1.向M、N中,分別通入x mol A和y mol B的混合氣體,初始M、N容積相同,保持溫度不變.下列說法正確的是( )
如圖所示,隔板Ⅰ固定不動,活塞Ⅱ可自由移動,M、N兩個容器中均發生反應:A(g)+3B(g)?2C(g)△H=-192kJ?mol-1.向M、N中,分別通入x mol A和y mol B的混合氣體,初始M、N容積相同,保持溫度不變.下列說法正確的是( )| A、若平衡時A氣體在兩容器中的體積分數相等,則x一定等于y |
| B、若x:y=1:2,則平衡時,M中的轉化率:A>B |
| C、若x:y=1:3,當M中放出熱量172.8 kJ時,A的轉化率為90% |
| D、若x=1.4,y=1,N中達到平衡時體積為2L,C為0.4mol,則反應起始時N的體積為2.6L |
| x-z |
| x+y-2z |
| a |
| x |
| 3a |
| 2x |
| 172.8kJ |
| 192kJ |
| 0.9 |
| x |
| 2.4mol |
| 2mol |
| 2L |
| VL |
| 5 |
| 3 |


 探究與鞏固河南科學技術出版社系列答案
探究與鞏固河南科學技術出版社系列答案科目:高中化學 來源: 題型:
| A、①②③④ | B、①②③ |
| C、②③④⑤⑥ | D、全部 |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
 對硝基苯甲酸在醫藥、感光材料等工業中應用廣泛.以對硝基甲苯等為原料制取對硝基苯甲酸(黃色結晶,熔點242℃,沸點約359℃,微溶于水,能升華.)的反應原理為:
對硝基苯甲酸在醫藥、感光材料等工業中應用廣泛.以對硝基甲苯等為原料制取對硝基苯甲酸(黃色結晶,熔點242℃,沸點約359℃,微溶于水,能升華.)的反應原理為: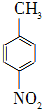 +Na2Cr2O7+4H2SO4→
+Na2Cr2O7+4H2SO4→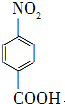 +Na2SO4+Cr2(SO4)3+5H2O
+Na2SO4+Cr2(SO4)3+5H2O查看答案和解析>>
科目:高中化學 來源: 題型:
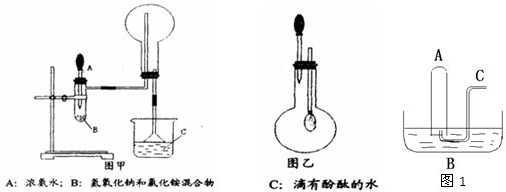
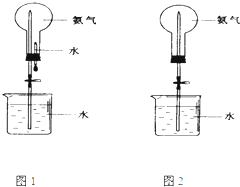 制取氨氣并完成噴泉實驗(圖中夾持裝置均已略去).
制取氨氣并完成噴泉實驗(圖中夾持裝置均已略去).查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
+ 4 |
+ 4 |
+ 4 |
| ||
查看答案和解析>>
科目:高中化學 來源: 題型:
| 溶解 |
| ① |
| BzCl2 |
| ② |
| NaOH |
| ③ |
| Na2CO3 |
| ④ |
| 過濾 |
| ⑤ |
| 適量鹽酸 |
| ⑥ |
| 蒸發、結晶、烘干 |
| ⑦ |
查看答案和解析>>
科目:高中化學 來源: 題型:
| 操作和現象 | 解釋 | |
| A | 向某鹵代烴在堿性條件下水解后的溶液中滴加硝酸銀溶液,有白色沉淀產生,證明該鹵代烴是氯代烴. | 因為氯代烴水解后的溶液中含Cl-,加入硝酸銀溶液產生AgCl白色沉淀. |
| B | 向溴水中加入苯充分振蕩,靜置分層,且水層幾乎無色. | 苯與溴水發生加成反應所以溴水褪色 |
| C | 要除去甲烷中混有的乙烯,可以將混合氣體通入到酸性高錳酸鉀溶液中,再通過濃硫酸干燥 | 因為乙烯可以被酸性高錳酸鉀溶液氧化,而甲烷不能被氧化. |
| D | 向蔗糖在酸性條件下水解的溶液中加NaOH溶液直至呈堿性,再加入新制的Cu(OH)2懸濁液,加熱,產生磚紅色沉淀. | 說明蔗糖水解產生了葡萄糖. |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com