
| A. | 鋅為負極,二氧化錳為正極 | |
| B. | 鋅為正極,二氧化錳為負極 | |
| C. | 工作時電子由二氧化錳經外電路流向鋅極 | |
| D. | 鋅電極發生還原反應,二氧化錳發生氧化反應 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:解答題
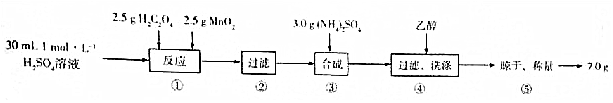
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 碳酸氫鈉與過量的氫氧化鈣溶液反應:HCO3-+OH-+Ca2+═CaCO3↓+H2O | |
| B. | 過氧化鈉與水的反應:2 O22-+2H2O═4 OH-+O2↑ | |
| C. | 碳酸鈣加入醋酸CO32-+2CH3COOH═CO2↑+2CH3COO-+H2O | |
| D. | 鐵與稀鹽酸的反應:2Fe+6H+═2Fe3++3H2↑ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | BaCl2溶液與Na2CO3溶液加足量稀醋酸 | |
| B. | Ba(OH)2溶液與KNO3溶液加足量H2SO4 | |
| C. | AgNO3溶液與Na2CO3溶液加足量稀硝酸 | |
| D. | Ca(OH)2溶液與FeCl3溶液加足量稀硝酸 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
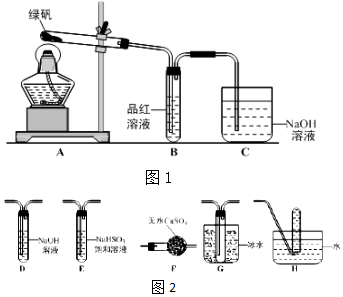
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 升高溫度可增大單位體積活化分子數百分數,促進有效碰撞,從而提高反應速率 | |
| B. | 增大體系壓強可增大單位體積活化分子數,促進有效碰撞,從而提高反應速率 | |
| C. | 放熱反應(△H<0)和熵增(△S>0)反應一定能自發反應 | |
| D. | 由能量守恒可知任何放熱反應都可設計成原電池 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| W | |||
| X | Y | Z |
| A. | 原子半徑大小:X>Y>Z | |
| B. | W、Y兩種元素都能與氧元素形成化合物WO2、YO2 | |
| C. | 最高價氧化物對應水化物的酸性:W>Y>Z | |
| D. | W元素的單質能從X的氧化物中置換出X單質 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com