
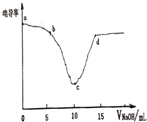
 電導率可用于衡量電解質溶液的導電能力,即電導率越大,則溶液的導電能力越強.利用電導率傳感器測得用0.100mol/L的NaOH溶液滴定10.00mL0.100mol/L的鹽酸,電導率曲線如圖所示.下列說法不正確的是( )
電導率可用于衡量電解質溶液的導電能力,即電導率越大,則溶液的導電能力越強.利用電導率傳感器測得用0.100mol/L的NaOH溶液滴定10.00mL0.100mol/L的鹽酸,電導率曲線如圖所示.下列說法不正確的是( )| A. | d點溶液中:c(Cl-)=2c(OH-)-2c(H+) | |
| B. | 電導率傳感器能用于酸堿中和滴定終點的判斷 | |
| C. | c點電導率最小是因為c點溶液的溶質為弱電解質 | |
| D. | c(Na+)、c(Cl-)對導電能力的影響比c(H+)、c(OH-)對導電能力的影響小 |
分析 A.任何電解質溶液中都存在電荷守恒、物料守恒,根據電荷守恒及物料守恒判斷;
B.HCl和NaOH反應方程式為HCl+NaOH=NaCl+H2O,根據圖象知,從0-10mL之間,隨著反應的進行,溶液中c(H+)濃度逐漸減小,溶液的電導率逐漸降低,加入溶液體積大于15mL時,溶液中氫氧根離子濃度逐漸增大,溶液的電導率增大,根據圖知,當恰好中和時電導率最小;
C.溶液電導率與離子濃度成正比,c點電導率低是因為離子濃度小;
D.HCl和NaOH反應方程式為HCl+NaOH=NaCl+H2O,根據圖象知,從0-10mL之間,隨著反應的進行,溶液中c(H+)濃度逐漸減小,溫度不變離子積常數不變,所以c(OH-)增大,但c(H+)、c(OH-)都較小,溶液的電導率逐漸降低;加入溶液體積大于15mL時,溶液中c(OH-)逐漸增大,溶液的電導率增大,從0-15mL過程中,c(Cl-)、c(Na+)始終大于c(H+)、c(OH-).
解答 解:A.任何電解質溶液中都存在電荷守恒、物料守恒,根據電荷守恒得c(Na+)+c(H+)=c(Cl-)+c(OH-),d點NaOH與HCl的體積之比為3:2,二者物質的量濃度相等,根據物料守恒得2c(Na+)=3c(Cl-),所以得c(Cl-)=2c(OH-)-2c(H+),
故A正確;
B.HCl和NaOH反應方程式為HCl+NaOH=NaCl+H2O,根據圖象知,從0-10mL之間,隨著反應的進行,溶液中c(H+)濃度逐漸減小,溶液的電導率逐漸降低,加入溶液體積大于15mL時,溶液中氫氧根離子濃度逐漸增大,溶液的電導率增大,根據圖知當恰好中和時電導率最小,所以可以電導率傳感器能用于酸堿中和滴定終點的判斷,故B正確;
C.電導率與離子濃度成正比,c點電導率低是因為離子濃度小,c點是二者恰好完全反應生成NaCl,NaCl是強電解質,故C錯誤;
D.HCl和NaOH反應方程式為HCl+NaOH=NaCl+H2O,根據圖象知,從0-10mL之間,隨著反應的進行,溶液中c(H+)濃度逐漸減小,溫度不變離子積常數不變,所以c(OH-)增大,但c(H+)、c(OH-)都較小,溶液的電導率逐漸降低;加入溶液體積大于15mL時,溶液中c(OH-)逐漸增大,溶液的電導率增大,從0-15mL過程中,c(Cl-)、c(Na+)始終大于c(H+)、c(OH-),由此可見c(Na+)、c(Cl-)對導電能力的影響比c(H+)、c(OH-)對導電能力的影響小,故D正確;
故選C.
點評 本題以電解質溶液的導電性為載體考查酸堿混合溶液定性判斷,明確反應實質、電導率的影響因素及混合溶液中溶質是解本題關鍵,會根據圖象中曲線變化獲取信息、加工信息,從而利用信息答題,易錯選項是A.


 字詞句篇與同步作文達標系列答案
字詞句篇與同步作文達標系列答案科目:高中化學 來源: 題型:選擇題
| A. | 1丙醇 | B. | 乙醇 | C. | 1丁醇 | D. | 1戊醇 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
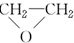 (環氧乙烷).
(環氧乙烷).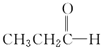 $\stackrel{NaBH_{4}}{→}$CH3CH2CH2OH
$\stackrel{NaBH_{4}}{→}$CH3CH2CH2OH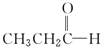 $→_{HCl}^{Zn(Hg)}$CH3CH2CH3
$→_{HCl}^{Zn(Hg)}$CH3CH2CH3查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 混合物 | 試劑 | 分離方法 | |
| A | 溴苯(溴) | 氫氧化鈉 | 分液 |
| B | 乙烷(乙烯) | 氫氣 | 催化劑、加熱 |
| C | 乙酸乙酯(乙酸) | 飽和碳酸鈉 | 分液 |
| D | 乙醇(水) | 生石灰 | 蒸餾 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 只有①和② | B. | 只有②③④ | C. | ①②③④ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
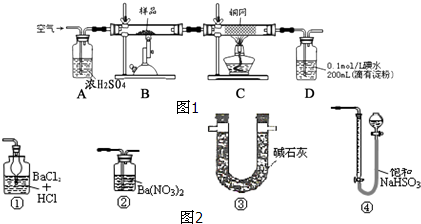
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 實驗步驟和結論(不要求寫具體操作過程): |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
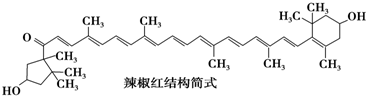
| A. | 不能發生氧化反應 | B. | 屬于芳香族化合物 | ||
| C. | 能發生消去反應 | D. | 分子中含有11個碳碳雙鍵 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com