
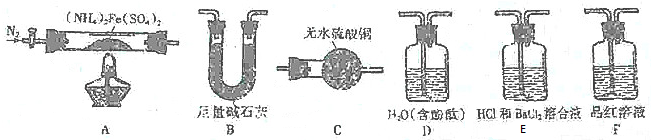
分析 (1)實驗I驗證分解產物中含有氨氣和水蒸氣,選擇裝置A先通入氮氣排凈裝置中的空氣,加熱分解硫酸亞鐵銨,分解產物中含有鐵氧化物、硫氧化物、氨氣和水蒸氣等,通過裝置C中無水硫酸銅檢驗生成的水,再通過裝置B中的足量堿石灰除去水蒸氣、硫的氧化物,通過裝置D檢驗氨氣的生成,通入后溶液變紅色說明生成氣體中含氨氣;
(2)證明水蒸氣生成是利用無水硫酸銅遇到水變藍色;
(3)證明有氨氣生成是利用氨氣極易溶于水生成一水合氨溶液顯堿性使酚酞變紅色;
(4)設計實驗利用亞鐵離子具有還原性可以使酸性高錳酸鉀溶液褪色設計;
(5)E中沒有明顯現象,說明無三氧化硫生成,F中溶液褪色說明有二氧化硫生成;
(6)最后裝置B是防止二氧化硫污染空氣;
(7)實驗證明(NH4)2Fe(SO4)2受熱分解生成氨氣、二氧化硫、氧化鐵、水,還有N2產生,結合原子守恒和電子守恒配平書寫化學方程式.
解答 解:(1)實驗I驗證分解產物中含有氨氣和水蒸氣,選擇裝置A先通入氮氣排凈裝置中的空氣,加熱分解硫酸亞鐵銨,分解產物中含有鐵氧化物、硫氧化物、氨氣和水蒸氣等,通過裝置C中無水硫酸銅檢驗生成的水,再通過裝置B中的足量堿石灰除去水蒸氣、硫的氧化物,通過裝置D檢驗氨氣的生成,通入后溶液變紅色說明生成氣體中含氨氣,所選用裝置的正確連接順序為ACBD,
故答案為:ACBD;
(2)利用無水硫酸銅遇到水變藍色證明水蒸氣生成,證明有水蒸氣生成的實驗現象為C中無水硫酸銅變藍色,
故答案為:C中無水硫酸銅變藍色;
(3)證明有氨氣生成是利用氨氣極易溶于水生成一水合氨,溶液顯堿性使酚酞變紅色,證明有氨氣生成的實驗現象為D中溶液變紅色,
故答案為:D中溶液變紅色;
(4)設計實驗證明A中殘留固體僅為Fe2O3,而不含FeO或Fe3O4,設計實驗利用亞鐵離子具有還原性可以使酸性高錳酸鉀溶液褪色設計,取少量A中殘留固體加入適量稀硫酸使其完全溶解,向溶液中滴加少量酸性高錳酸鉀溶液,若高錳酸鉀溶液不褪色,則殘留固體是Fe2O3而不含FeO和Fe3O4,
故答案為:取少量A中殘留固體加入適量稀硫酸使其完全溶解,向溶液中滴加少量酸性高錳酸鉀溶液,若高錳酸鉀溶液不褪色,則殘留固體是Fe2O3而不含FeO和Fe3O4;
(5)E中含HCl的BaCl2溶液沒有明顯現象,說明無硫酸鋇沉淀生成,證明分解產物中無三氧化硫生成,二氧化硫具有漂白性能使品紅溶液褪色,F中溶液褪色說明有二氧化硫生成,
故答案為:分解產物中有SO2沒有SO3;
(6)連接裝置A-E-F-B進行實驗,最后裝置B是防止二氧化硫污染空氣,
故答案為:吸收SO2防止污染空氣;
(7)實驗證明(NH4)2Fe(SO4)2受熱分解生成氨氣、二氧化硫、氧化鐵、水,還有N2產生,結合原子守恒和電子守恒配平書寫化學方程式為:2(NH4)2Fe(SO4)2$\frac{\underline{\;500℃\;}}{\;}$Fe2O3+4SO2↑+2NH3↑+N2↑+5H2O,
故答案為:2(NH4)2Fe(SO4)2$\frac{\underline{\;500℃\;}}{\;}$Fe2O3+4SO2↑+2NH3↑+N2↑+5H2O.
點評 本題考查了物質組成的實驗探究和實驗設計,主要是實驗基本操作、物質性質的理解應用,掌握基礎是解題關鍵,題目難度中等.


科目:高中化學 來源: 題型:選擇題
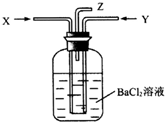 碳跟濃硫酸共熱產生的混合氣體X(CO2、SO2)和銅跟過量濃硝酸反應產生的氣體Y(NO2)同時通入盛有足量氯化鋇溶液的洗氣瓶中(如圖裝置),下列有關說法正確的是( )
碳跟濃硫酸共熱產生的混合氣體X(CO2、SO2)和銅跟過量濃硝酸反應產生的氣體Y(NO2)同時通入盛有足量氯化鋇溶液的洗氣瓶中(如圖裝置),下列有關說法正確的是( )| A. | 洗氣瓶中產生的沉淀是碳酸鋇 | B. | 在Z導管出來的氣體中無二氧化碳 | ||
| C. | 在Z導管口不會出現紅棕色氣體 | D. | 洗氣瓶中產生的沉淀是硫酸鋇 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | HCl的水溶液是強酸,HBr的水溶液也是強酸 | |
| B. | CO2氣體通入Ba(NO3)2溶液中不反應,SO2氣體通入Ba(NO3)2溶液中也不反應 | |
| C. | O2與Cu反應生成CuO,S與Cu反應生成CuS | |
| D. | CaCO3與稀硝酸反應生成CO2,CaSO3與稀硝酸反應生成SO2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
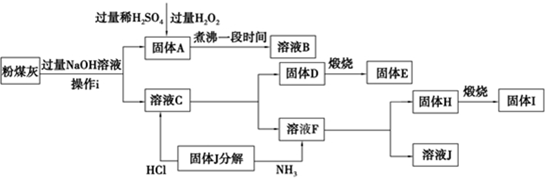
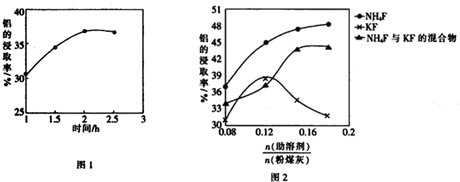
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ②③⑤ | B. | ③④⑤ | C. | ②④⑤ | D. | ①②③ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 兩種粒子,若核外電子排布完全相同,則其化學性質一定相同 | |
| B. | 離子化合物中,一定存在金屬元素和非金屬元素 | |
| C. | 同時含有離子鍵和共價鍵的化合物,一定是離子化合物,不可能是共價化合物 | |
| D. | 難失電子的原子,獲得電子的能力一定強 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
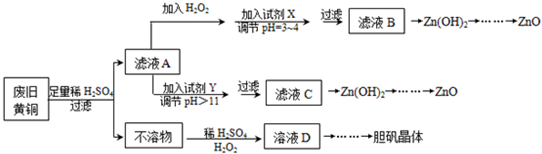
| Fe3+ | Fe2+ | Zn2+ | |
| 開始沉淀的pH | 1.1 | 5.8 | |
| 沉淀完全的pH | 3.0 | 8.8 | 8.9 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
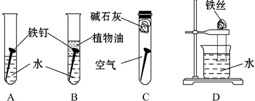 某研究性學習小組對鐵生銹進行研究.
某研究性學習小組對鐵生銹進行研究.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com