
| A. | 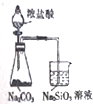 驗證碳酸與硅酸的酸性 | B. | 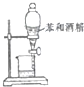 分離苯和酒精 | ||
| C. | 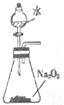 制取少量O2 | D. | 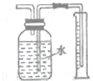 收集少量NO2氣體 |
分析 A.鹽酸易揮發,鹽酸與硅酸鈉反應;
B.苯和酒精互溶;
C.過氧化鈉與水反應生成氧氣,利用活塞控制水的加入;
D.二氧化氮與水反應.
解答 解:A.鹽酸易揮發,鹽酸與硅酸鈉反應,則圖中裝置不能比較碳酸、硅酸的酸性,故A錯誤;
B.苯和酒精互溶,不能利用圖中分液裝置分離,應選蒸餾法,故B錯誤;
C.過氧化鈉與水反應生成氧氣,利用活塞控制水的加入,則可制備少量氧氣,故C正確;
D.二氧化氮與水反應,圖中裝置不能收集少量NO2氣體,故D錯誤;
故選C.
點評 本題考查化學實驗方案的評價,為高頻考點,把握圖中實驗裝置的作用、物質的制備、混合物分離、酸性比較為解答的關鍵,側重分析與實驗能力的考查,注意元素化合物知識的應用及實驗評價性分析,題目難度不大.


 名校提分一卷通系列答案
名校提分一卷通系列答案 課程達標測試卷闖關100分系列答案
課程達標測試卷闖關100分系列答案 新卷王期末沖刺100分系列答案
新卷王期末沖刺100分系列答案 全能闖關100分系列答案
全能闖關100分系列答案科目:高中化學 來源: 題型:多選題
| 容器編號 | 起始時各物質物質的量/mol | 達平衡時體系能量的變化 | ||
| N2 | H2 | NH3 | ||
| ① | 1 | 3 | 0 | 放出熱量:23.15kJ |
| ② | 0.9 | 2.7 | 0.2 | 放出熱量:Q |
| A. | 容器①、②中反應的平衡常數相等 | |
| B. | 平衡時,兩個容器中NH3的體積分數均為25% | |
| C. | 容器②中達平衡時放出的熱量Q=23.15 kJ | |
| D. | 若容器①體積為0.5L,則平衡時放出的熱量<23.15kJ |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 22.4 L CO和CO2的混合氣體中所含的碳原子數一定是NA | |
| B. | 標準狀況下,22.4 L氖氣含有原子數為NA | |
| C. | 物質的量濃度為2 mol/L的BaCl2溶液中,含有Cl-個數為4NA | |
| D. | 標準狀況下,11.2 L H2O含有0.5NA分子 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 離子的還原性強弱:I->Fe2+>Br- | |
| B. | 當a≥b時,發生的離子反應:2I-+Br2═I2+2Br- | |
| C. | 當5a=4b時,反應后的離子濃度之比:c(Fe2+):c(Fe3+):c(Br-)=1:1:5 | |
| D. | 當3a≤2b時,發生的離子反應:2Fe2++2I-+2Br2═2Fe3++I2+4Br- |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com