
| A、反應熱和焓變的單位都是kJ | B、如果反應是在恒溫恒壓條件下進行的,此時的反應熱與焓變相等 | C、如果反應是在恒溫恒容條件下進行的,此時的反應熱與焓變相等 | D、任何化學反應的反應熱均可通過實驗直接測定 |
科目:高中化學 來源: 題型:
| A、Ag+和Cl-在水溶液中的反應,其活化能為零 | B、化學反應的反應熱只與反應體系的始態和終點狀態有關,而與反應的途徑無關 | C、放熱反應一定能自發進行,而吸熱反應一定不能自發進行 | D、熵增大的反應其焓變不一定增大,焓變增大的反應其熵不一定增大 |
查看答案和解析>>
科目:高中化學 來源:2011-2012年黑龍江大慶鐵人中學高一下學期期中考試化學試卷(帶解析) 題型:填空題
(10分)試回答下列各問題:
(1)如圖Ⅰ所示是1 mol NO2和CO反應生成 CO2和NO過程中能量變化示意圖,請寫出NO2和CO反應的熱化學方程式: 。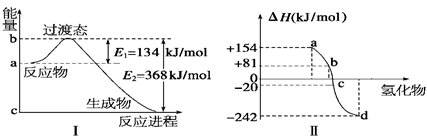
(2)化學反應的焓變與反應物和生成物的鍵能有關。
①已知:H2(g)+Cl2(g) ="==" 2HCl(g) ΔH="-185" kJ/mol;
鍵能ΔH298(H—H)="436" kJ/mol,ΔH298(Cl—Cl)="247" kJ/mol,則ΔH298(H—Cl)= 。
②圖Ⅱ表示氧族元素中的氧、硫、硒(Se)、碲生成氫化物時的焓變數據,根據這組焓變數據可確定a、b、c、d分別代表的元素,試寫出硒化氫發生分解反應的熱化學方程式: 。
(3)已知: ①Fe2O3(s)+3CO(g)  2Fe(s)+3CO2(g) ΔH="-a" kJ/mol
2Fe(s)+3CO2(g) ΔH="-a" kJ/mol
②3Fe2O3(s)+CO(g)  2Fe3O4(s)+CO2(g) ΔH="-b" kJ/mol
2Fe3O4(s)+CO2(g) ΔH="-b" kJ/mol
③Fe3O4(s)+CO(g)  3FeO(s)+CO2(g) ΔH="+ckJ/mol"
3FeO(s)+CO2(g) ΔH="+ckJ/mol"
則FeO(s) +CO(g)  Fe(s)+CO2(g) ΔH=- 。
Fe(s)+CO2(g) ΔH=- 。
查看答案和解析>>
科目:高中化學 來源:2011-2012年黑龍江大慶鐵人中學高一下學期期中考試化學試卷(解析版) 題型:填空題
(10分)試回答下列各問題:
(1)如圖Ⅰ所示是1 mol NO2和CO反應生成 CO2和NO過程中能量變化示意圖,請寫出NO2和CO反應的熱化學方程式: 。
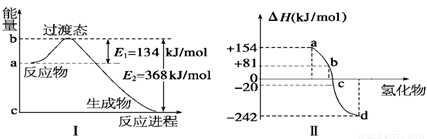
(2)化學反應的焓變與反應物和生成物的鍵能有關。
①已知:H2(g)+Cl2(g) === 2HCl(g) ΔH=-185 kJ/mol;
鍵能ΔH298(H—H)=436 kJ/mol,ΔH298(Cl—Cl)=247 kJ/mol,則ΔH298(H—Cl)= 。
②圖Ⅱ表示氧族元素中的氧、硫、硒(Se)、碲生成氫化物時的焓變數據,根據這組焓變數據可確定a、b、c、d分別代表的元素,試寫出硒化氫發生分解反應的熱化學方程式: 。
(3)已知: ①Fe2O3(s)+3CO(g)
 2Fe(s)+3CO2(g) ΔH=-a
kJ/mol
2Fe(s)+3CO2(g) ΔH=-a
kJ/mol
②3Fe2O3(s)+CO(g)
 2Fe3O4(s)+CO2(g)
ΔH=-b kJ/mol
2Fe3O4(s)+CO2(g)
ΔH=-b kJ/mol
③Fe3O4(s)+CO(g)
 3FeO(s)+CO2(g) ΔH=+ckJ/mol
3FeO(s)+CO2(g) ΔH=+ckJ/mol
則FeO(s) +CO(g)  Fe(s)+CO2(g) ΔH=-
。
Fe(s)+CO2(g) ΔH=-
。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com