
| A. | Z單質還原性大于Y單質 | |
| B. | X的氫化物沸點高于W的氫化物 | |
| C. | 僅含X、Y兩元素的化合物均只含離子鍵 | |
| D. | 上述四種元素形成的簡單離子中,X離子半徑最小 |
分析 Y、Z、W的最高價氧化物對應水化物間可兩兩反應生成鹽和水,說明這三種元素的最高價化合物的水化物有強酸、強堿和兩性氫氧化物,Z的原子序數小于W而大于Y,所以Z是Al元素,Y為Na元素,化合物YWX是漂白液的有效成分,應為NaClO,則X為O元素,W為Cl元素,結合物質的性質分析解答.
解答 解:Y、Z、W的最高價氧化物對應水化物間可兩兩反應生成鹽和水,說明這三種元素的最高價化合物的水化物有強酸、強堿和兩性氫氧化物,Z的原子序數小于W而大于Y,所以Z是Al元素,Y為Na元素,化合物YWX是漂白液的有效成分,應為NaClO,則X為O元素,W為Cl元素,
A.金屬性Na大于Al,Na的還原性較強,故A錯誤;
B.水可形成氫鍵,沸點較高,故B正確;
C.僅含X、Y兩元素的化合物如為過氧化鈉,則含有共價鍵,故C錯誤;
D.核外電子排布相同的離子,核電荷數越大離子半徑越小,鋁離子半徑最小,故D錯誤.
故選B.
點評 本題考查了元素位置結構性質的關系及應用,熟悉元素周期表及原子結構是解本題關鍵,再結合元素周期律、物質的性質來分析解答,題目難度不大.


科目:高中化學 來源: 題型:多選題
| A. | 探究催化劑對H2O2分解速率的影響:在相同條件下,向一試管中加入2mL5%H2O2和1mLH2O,向另一試管中加入2mL 10%H2O2和1mLFeCl3溶液,觀察并比較實驗現象 | |
| B. | 提純含有少量乙酸的乙酸乙酯:向含有少量乙酸的乙酸乙酯中加入過量飽和碳酸鈉溶液,振蕩后靜置分液,并除去有機相的水 | |
| C. | 檢驗溶液中是否含有Fe3+:取少量待檢驗溶液,向其中加入少量新制氯水,再滴加KSCN溶液,觀察實驗現象 | |
| D. | 制備Al(OH)3懸濁液:向1mol•L-1AlCl3溶液中加過量的6mol•L-1NaOH溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
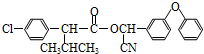 )
)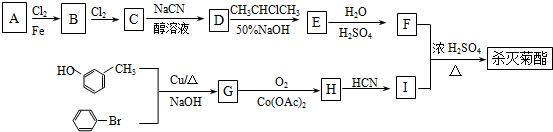
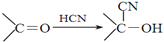
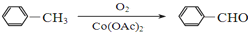
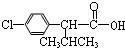 +
+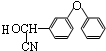 $→_{△}^{濃硫酸}$
$→_{△}^{濃硫酸}$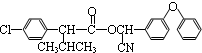 +H2O.
+H2O.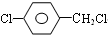 +3NaOH$→_{△}^{H_{2}O}$2NaCl+H2O+
+3NaOH$→_{△}^{H_{2}O}$2NaCl+H2O+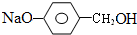 .
.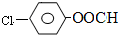 結構,則符合此條件的F共有8種.
結構,則符合此條件的F共有8種.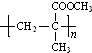 (用合成路線流程圖表示,并注明反應條件).
(用合成路線流程圖表示,并注明反應條件).查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 熱穩定性H2O>H2S | B. | 還原性Ⅰ->Br->Cl- | ||
| C. | 金屬性 K>Na | D. | 酸性 HCl>HF |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
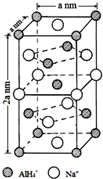 氫化鋁鈉(NaAlH4)是一種新型輕質儲氫材料,摻入少量Ti的NaAlH4在150℃時釋氫,在170℃、15,.2MPa條件下又重復吸氫.NaAlH4可由AlCl3和NaH在適當條件下合成.NaAlH4的晶胞結構如圖所示.
氫化鋁鈉(NaAlH4)是一種新型輕質儲氫材料,摻入少量Ti的NaAlH4在150℃時釋氫,在170℃、15,.2MPa條件下又重復吸氫.NaAlH4可由AlCl3和NaH在適當條件下合成.NaAlH4的晶胞結構如圖所示. .
. (標明配位鍵).
(標明配位鍵).查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 實驗操作 | 實驗目的 | |
| A | 將潮濕的NH3通過盛有無水CaCl2的干燥管 | 除去NH3中的水蒸氣 |
| B | 往鐵和稀硝酸反應后的溶液中滴入KSCN溶液 | 驗證溶液中是否含有Fe3+ |
| C | 甲基橙作指示劑,用標準NaOH溶液滴定鹽酸至紅色 | 測量鹽酸物質的量濃度 |
| D | 向2ml0.2mol/L的AgNO3溶液中先后滴加0.2mol/L 的NaCl溶液、KBr溶液各5滴 | 確定AgCl、AgBr的Kap的相對大小 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
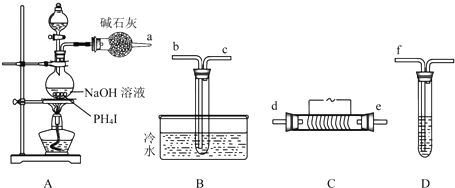
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
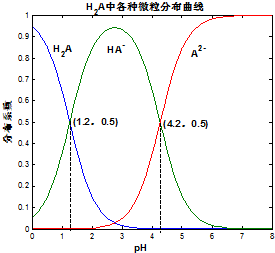 常溫下 0.1mol/L的H2A溶液中H2A、HA-、A2- 三者中所占物質的量分數(分布系數)隨pH變化的關系如圖所示.下列表述不正確的是( )
常溫下 0.1mol/L的H2A溶液中H2A、HA-、A2- 三者中所占物質的量分數(分布系數)隨pH變化的關系如圖所示.下列表述不正確的是( )| A. | H2A?2H++A2- K=10-5.4 | |
| B. | 在 0.1mol/L NaHA溶液中,各離子濃度大小關系為:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) | |
| C. | 已知25℃時HF的 Ka=10-3.45,將少量H2A的溶液加入足量NaF溶液中,發生的反應為:H2A+F-═HF+HA- | |
| D. | 將等物質的量的NaHA、Na2A溶于水中,所得溶液pH恰好為4.2 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com