
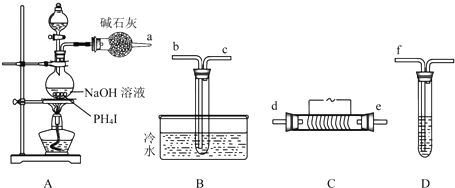
分析 制取磷化氫并驗證其性質實驗流程:乙醚(無色液體,沸點34.5℃,微溶于水,不與Fe2( S04)3反應),乙醚為易揮發的有機溶劑,實驗開始時,先從分液漏斗向盛有PH4I的圓底燒瓶中加入過量乙醚,并微熱數分鐘,目的是將空氣排盡,以防止PH3在裝置中燃燒(或自燃),提供惰性氣體環境,再從分液漏斗向圓底燒瓶中加入一定量的濃NaOH溶液繼續加熱,發生反應PH4I+NaOH$\frac{\underline{\;\;△\;\;}}{\;}$PH3↑+NaI+H2O,在裝置C處用電熱器控制溫度在300℃左右,發生反應:4PH3$\frac{\underline{\;300℃\;}}{\;}$P4+6H2(或2PH3$\frac{\underline{\;300℃\;}}{\;}$2P+3H2),B裝置的試管中有白色蠟狀固體生成為白磷,D裝置的試管中Fe2(SO4)3溶液顏色由棕黃色變成淡綠色,說明生成+2價的鐵,磷化氫具有還原性,發生反應:4PH3+12Fe3+=P4↓+12Fe2++12H+(或 PH3+3Fe3+=P↓+3Fe2++3H+),同時也有白色蠟狀固體白磷生成.
(1)根據實驗目的先排裝置中的空氣,防止反應物磷化氫、生成物白磷燃燒,然后,加入氫氧化鈉,制取硫化氫,硫化氫分解,B觀察反應的產物,最后檢驗鐵離子和磷化氫的反應,據此連接裝置;
(2)N與P處在同一主族,根據碘化氨合堿的反應書寫反應方程式;
(3)乙醚為易揮發的有機溶劑,實驗開始時,先從分液漏斗向盛有PH4I的圓底燒瓶中加入過量乙醚,并微熱數分鐘,目的是將空氣排盡;
(4)磷化氫受熱分解生成白磷、氫氣,磷化氫和鐵離子發生氧化還原反應生成亞鐵離子和白磷;
(5)裝置B中磷化氫受熱分解,說明磷化氫不穩定,裝置C中磷化氫能將鐵離子還原成亞鐵離子,說明其具有還原性;
(6)磷化氫、氫氣都能燃燒,可通過燃燒的方法進行尾氣處理.
解答 解:制取磷化氫并驗證其性質實驗流程:乙醚(無色液體,沸點34.5℃,微溶于水,不與Fe2( S04)3反應),乙醚為易揮發的有機溶劑,實驗開始時,先從分液漏斗向盛有PH4I的圓底燒瓶中加入過量乙醚,并微熱數分鐘,目的是將空氣排盡,以防止PH3在裝置中燃燒(或自燃),提供惰性氣體環境,再從分液漏斗向圓底燒瓶中加入一定量的濃NaOH溶液繼續加熱,發生反應PH4I+NaOH$\frac{\underline{\;\;△\;\;}}{\;}$PH3↑+NaI+H2O,在裝置C處用電熱器控制溫度在300℃左右,發生反應:4PH3$\frac{\underline{\;300℃\;}}{\;}$P4+6H2(或2PH3$\frac{\underline{\;300℃\;}}{\;}$2P+3H2),B裝置的試管中有白色蠟狀固體生成為白磷,D裝置的試管中Fe2(SO4)3溶液顏色由棕黃色變成淡綠色,說明生成+2價的鐵,磷化氫具有還原性,發生反應:4PH3+12Fe3+=P4↓+12Fe2++12H+(或 PH3+3Fe3+=P↓+3Fe2++3H+),同時也有白色蠟狀固體白磷生成.
(1)B裝置的試管中有白色蠟狀固體生成為白磷,連接順序為a→d、e(或e、d),檢驗磷化氫的還原性,D裝置的試管中Fe2(SO4)3溶液顏色由棕黃色變成淡綠色,說明生成+2價的鐵,連接順序為b、c→f,
故答案為:d、e、b、c (或 e、d、b、c);
(2)銨鹽和堿反應生成氨氣,N與P處在同一主族,磷鹽和堿反應生成磷化氫,反應為PH4I+NaOH$\frac{\underline{\;\;△\;\;}}{\;}$PH3↑+NaI+H2O,
故答案為:PH4I+NaOH$\frac{\underline{\;\;△\;\;}}{\;}$PH3↑+NaI+H2O;
(3)PH3在空氣中易燃燒(或自燃),裝置中若空氣不排盡,會自燃,所以實驗開始時,先向圓底燒瓶中加入乙醚并微熱數分鐘,其目的是將空氣排盡,以防止PH3在裝置中燃燒(或自燃),
故答案為:將空氣排盡,以防止PH3在裝置中燃燒(或自燃);
(4)由上述分析可知,C中發生4PH3$\frac{\underline{\;300℃\;}}{\;}$P4+6H2,D中離子反應為4PH3+12Fe3+=P4↓+12Fe2++12H+,
故答案為:4PH3$\frac{\underline{\;300℃\;}}{\;}$P4+6H2;4PH3+12Fe3+=P4↓+12Fe2++12H+;
(5)B裝置的試管中有白色蠟狀固體生成為白磷,為磷化氫受熱分解生成的產物,說明磷化氫不穩定,裝置C中磷化氫能將鐵離子還原成亞鐵離子4PH3+12Fe3+=P4↓+12Fe2++12H+(或 PH3+3Fe3+=P↓+3Fe2++3H+),說明其具有還原性,
故答案為:BC;
(6)磷化氫有毒,需進行尾氣處理,磷化氫、氫氣都能燃燒,可通過燃燒的方法進行尾氣處理,硫化氫與硫酸銅溶液能反應,
故答案為:將尾氣點燃或通入到CuSO4溶液.
點評 本題考查制備實驗方案的設計,為高頻考點,把握制備實驗原理、實驗裝置的作用、習題中的信息為解答的關鍵,側重分析與實驗能力的綜合考查,題目難度中等.


 備戰中考寒假系列答案
備戰中考寒假系列答案科目:高中化學 來源: 題型:解答題
 高中化學教材介紹了鈉、鎂、鋁、鐵、氯、硫、氮、硅等元素及其化合物的知識,是其它化學知識的載體.
高中化學教材介紹了鈉、鎂、鋁、鐵、氯、硫、氮、硅等元素及其化合物的知識,是其它化學知識的載體.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Z單質還原性大于Y單質 | |
| B. | X的氫化物沸點高于W的氫化物 | |
| C. | 僅含X、Y兩元素的化合物均只含離子鍵 | |
| D. | 上述四種元素形成的簡單離子中,X離子半徑最小 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在常溫常壓下,2.24LSO2與O2混合氣體中所含氧原子數為0.2NA | |
| B. | 50mL12mol/L鹽酸與足量MnO2共熱,轉移的電子數為0.3NA | |
| C. | 氫氧燃料電池正極消耗22.4L(標準狀況)氣體時,電路中通過的電子數目為2NA | |
| D. | 標準狀況下,20gD20分子中所含中子數為10NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | KNO3 | B. | K2CO3 | C. | HNO3 | D. | Na2SO4 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | “山東疫苗案”涉疫苗未冷藏儲運而失效,這與蛋白質變性有關 | |
| B. | 硫、氮、碳的氧化物是形成酸雨的主要物質 | |
| C. | 半導體行業中有一句“行話”:“從沙灘到用戶”,說明計算機芯片的主要成分是二氧化硅 | |
| D. | 自來水廠常用明礬作消毒殺菌劑 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 某校化學興趣小組探究SO2與FeCl3溶液的反應,所用裝置如圖所示(夾持儀器已略去).
某校化學興趣小組探究SO2與FeCl3溶液的反應,所用裝置如圖所示(夾持儀器已略去).查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com