
| A. |
| |||||||||
| B. |
| |||||||||
| C. | 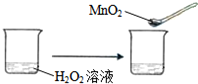 | |||||||||
| D. | 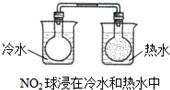 |
分析 平衡移動原理:如果改變影響平衡的一個條件(如濃度、壓強或溫度等),平衡就向能夠減弱這種改變的方向移動,平衡移動原理適用的對象應存在可逆過程,如與可逆過程無關,則不能用平衡移動原理解釋,平衡移動原理對所有的動態平衡都適用.
解答 解:A、氯水的濃度縮小一倍,PH減小不到一個單位,說明加水稀釋過程,促進氯氣和水的反應的平衡的移動,所以符合勒夏特列原理,故A不選;
B、水的電離是吸熱過程,升高溫度促進電離,所以水的離子積常數變大,所以符合勒夏特列原理,故B不選;
C、使用催化劑平衡不移動,所以不符合勒夏特列原理,故C選;
D、二氧化氮轉化為四氧化二氮是放熱反應,所以放在熱水中,平衡向生成二氧化氮方向移動,所以顏色加深,符合勒夏特列原理,故D不選;
故選C.
點評 本題考查化學平衡移動原理,為高頻考點,明確化學平衡移動原理內涵及適用范圍是解本題關鍵,注意:平衡移動原理只適用于“改變條件時能引起平衡移動的化學反應”,題目難度不大.


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:選擇題
| A. | 24g鎂的原子最外層電子數為NA | |
| B. | 0.3mol O2與一定量的Fe3+在一定條件下完全反應,生成Fe2O3和Fe3O4的混合物,則轉移電子數為1.2mol | |
| C. | 2L 0.1mol/L氯化鐵溶液中含有Fe的數目為0.2NA | |
| D. | 1L水中溶解了58.5gNaCl,該溶液的物質的量濃度為1mol/L |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 實驗操作 | 實驗目的或結論 |
| A | 向FeCl2溶液中通入Cl2,然后滴加KSCN溶液 | 驗證Cl2的氧化性比Fe3+強 |
| B | 向某溶液中加入鹽酸酸化的氯化鋇溶液,有白色沉淀生成 | 該溶液中不一定含有SO42- |
| C | 用潔凈的玻璃棒蘸取某溶液進行焰色反應,火焰呈黃色 | 該溶液中一定含有Na+,一定無K+ |
| D | 將某氣體通入品紅溶液中,溶液褪色 | 該氣體中一定含有SO2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鎂和稀硫酸:Mg+2H+═Mg2++H2↑ | |
| B. | 硅和燒堿溶液:Si+2OH-+H2O═SiO32-+2H2↑ | |
| C. | NaHCO3溶液和足量Ca(OH)2溶液Ca2++HCO3-+OH-═CaCO3↓+H2O | |
| D. | 氯化鋁溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
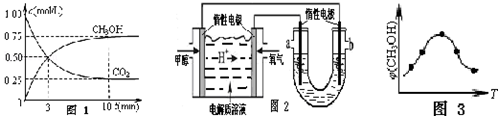
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 濃硝酸中加入過量鐵粉并加熱:Fe+3NO3-+6H+$\frac{\underline{\;\;△\;\;}}{\;}$Fe3++3NO2↑+3H2O | |
| B. | 硫酸銅溶液與氫氧化鋇溶液反應:Ba2++SO42-=BaSO4↓ | |
| C. | 等體積等物質的量濃度的氫氧化鋇溶液與碳酸氫銨溶液混合:Ba2++2 OH-+NH4++HCO3-═BaCO3↓+NH3•H2O+H2O | |
| D. | 用FeCl3溶液腐蝕印刷電路板:Fe3++Cu═Fe2++Cu2+ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | a管發生吸氧腐蝕,b管發生析氫腐蝕 | |
| B. | a處溶液的pH增大,b處溶液的pH減小 | |
| C. | 一段時間后,a管液面高于b管液面 | |
| D. | 兩側生鐵絲發生相同的電極反應:Fe-2e-═Fe2+ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 常溫下,pH均等于4的硫酸溶液與醋酸溶液,兩種溶液中c(SO42-)與c(CH3COO-)之比為1:2 | |
| B. | 常溫下,向pH=4.0的醋酸溶液中加入水稀釋后,溶液中c(H+)和c(OH-)都將變小 | |
| C. | 常溫下,0.1mol/L NaHA溶液的PH=5,溶液:c(HA-)>c(H+)>c(H2A)>c(A2-) | |
| D. | 0.1mol•L-1的(NH4)2Fe(SO4)2溶液中:c(NH4+)=c(SO42-)>c(Fe2+)>c(H+) |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com