
| A. | Na+、OH-、S2O${\;}_{3}^{2-}$、Cl- | B. | Fe2+、K+、H+、NO${\;}_{3}^{-}$ | ||
| C. | H+、C2O${\;}_{4}^{2-}$、MnO${\;}_{4}^{-}$、SO${\;}_{4}^{2-}$ | D. | Na+、Ca2+、AlO${\;}_{2}^{-}$、HCO${\;}_{3}^{-}$ |
 每課必練系列答案
每課必練系列答案科目:高中化學 來源: 題型:選擇題
 甲圖為一種新型污水處理裝置,該裝置可利用一種微生物將有機廢水的化學能直接轉化為電能.乙圖是一種家用環保型消毒液發生器,用惰性電極電解飽和食鹽水.下列說法中正確的是( )
甲圖為一種新型污水處理裝置,該裝置可利用一種微生物將有機廢水的化學能直接轉化為電能.乙圖是一種家用環保型消毒液發生器,用惰性電極電解飽和食鹽水.下列說法中正確的是( )| A. | 裝置乙的b極要與裝置甲的X極連接 | |
| B. | 裝置乙中a極的電極反應式為2Cl--2e-═Cl2↑ | |
| C. | 若有機廢水中主要含有葡萄糖,則裝置甲中M的電極反應式為:C6H12O6+6H2O-24e-═6CO2↑+24H+ | |
| D. | N電極發生還原反應,當N電極消耗56 L氣體(標準狀況下)時,則有2NA個H+通過離子交換膜 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

 ,屬于弱電解質的是H2O、Al(OH)3.
,屬于弱電解質的是H2O、Al(OH)3.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 古代發明 | 化學變化 |
| A | 生產陶瓷 | SiO2+CaCO3 $\frac{\underline{\;高溫\;}}{\;}$CaSiO3+CO2↑ |
| B | 黑火藥爆炸 | S+2KNO3+3C$\frac{\underline{\;點燃\;}}{\;}$K2S+N2↑+3CO2↑ |
| C | 濕法煉銅 | CuSO4+Fe═Cu+FeSO4 |
| D | 用谷物釀酒 | (C6H10O5)n→C6H12O6→CH3CH2OH |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 已知A、B、C、D、E、F六種化合物均由上述元素中的幾種組成,它們之間的關系如圖所示,A為淡黃色固體,B是常見液體,D是兩性氧化物,F是引起酸雨的主要氣體.
已知A、B、C、D、E、F六種化合物均由上述元素中的幾種組成,它們之間的關系如圖所示,A為淡黃色固體,B是常見液體,D是兩性氧化物,F是引起酸雨的主要氣體.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1mol甲基中含電子數目為10NA | |
| B. | 標準狀況下,11.2L己烷所含有的分子數為0.5NA | |
| C. | 14g乙烯和丁烯的混合物中含有的原子總數為3NA個 | |
| D. | 常溫下,4gCH4含有2NA個C-H共價鍵 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
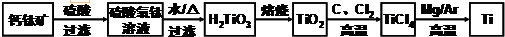
 ,其原子核外共有22種運動狀態不相同的電子.金屬鈦晶胞如圖1所示,為六方最密堆積(填堆積方式).
,其原子核外共有22種運動狀態不相同的電子.金屬鈦晶胞如圖1所示,為六方最密堆積(填堆積方式).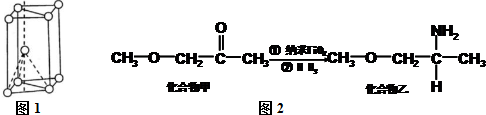

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 可逆反應的化學反應速率是指正反應速率 | |
| B. | 在可逆反應里正反應的速率是正值,逆反應的速率是負值 | |
| C. | 在一定條件下,當可逆反應的正反應速率與逆反應速率相等時,反應物和生成物的濃度不再發生變化,這就是該反應所達到的限度 | |
| D. | 對于可逆反應來說,反應物轉化為生成物沒有一定的限度 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | a>b | B. | a<b | C. | a=b | D. | 無法確定 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com