
| A. | 原子半徑:rW>rZ>rY | |
| B. | 化合物X2Y、ZY、ZX2中化學鍵的類型相同 | |
| C. | 由X、Y、Z、W組成的化合物的水溶液可能顯酸性 | |
| D. | 由Y元素形成的離子與W元素形成的離子的電子數不可能相同 |
分析 X、Y、Z、W是原子序數依次增大的短周期主族元素,X是周期表中原子半徑最小的元素,則X為H元素;Y的次外層電子數是最外層的$\frac{1}{3}$,原子只能有2個電子層,最外層電子數為6,故Y為O元素;W與Y屬于同一主族,則W為S元素;ZX2是一種儲氫材料,Z表現+2價,結合原子序數可知Z為Mg,結合元素周期律以及元素化合物結構與性質解答.
解答 解:X、Y、Z、W是原子序數依次增大的短周期主族元素,X是周期表中原子半徑最小的元素,則X為H元素;Y的次外層電子數是最外層的$\frac{1}{3}$,原子只能有2個電子層,最外層電子數為6,故Y為O元素;W與Y屬于同一主族,則W為S元素;ZX2是一種儲氫材料,Z表現+2價,結合原子序數可知Z為Mg.
A.同周期從左向右原子半徑在減小,同主族自上而下原子半徑增大,則原子半徑為Z(Mg)>W(S)>R(O),故A錯誤;
B.化合物H2O含有共價鍵,MgO含有離子鍵,MgH2中含有離子鍵,故B錯誤;
C.由X、Y、Z、W組成的化合物為MgSO4.7H2O等,溶液中鎂離子水解,溶液呈酸性,故C正確;
D.由Y元素形成的O22-,核外電子數為18,W元素形成的S2-離子核外電子數也是18,故D錯誤.
故選:C.
點評 本題考查結構性質位置關系應用,注意對元素周期律的理解掌握,D選項為易錯點,學生容易忽略過氧根離子.


科目:高中化學 來源: 題型:選擇題
| A. | 1:3 | B. | 1:2 | C. | 3:1 | D. | 3:2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
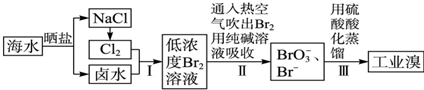
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 44 g CO2 氣體中含有原子數為2NA | |
| B. | 常溫常壓下22.4 L H2 中含原子數為2NA | |
| C. | 64g二氧化硫含有原子數為3NA | |
| D. | 標準狀況下22.4 L H2O中含分子數為NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

 ;該物質溶于水后的溶液呈堿性(填“酸”、“堿”或“中”).
;該物質溶于水后的溶液呈堿性(填“酸”、“堿”或“中”). .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
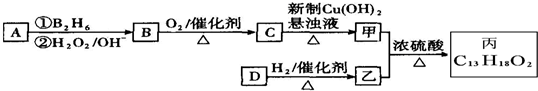
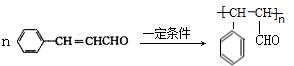 .
. .
. .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 A、B、C、D、E五種短周期元素,原子序數E>D>A>B>C,且A、B、D、E同周期,A、C同主族,A的原子結構示意圖如圖,B的最外層電子數比K層電子多1,D元素的主族序數是周期序數的2倍,E的單質是黃綠色氣體;據此填空:
A、B、C、D、E五種短周期元素,原子序數E>D>A>B>C,且A、B、D、E同周期,A、C同主族,A的原子結構示意圖如圖,B的最外層電子數比K層電子多1,D元素的主族序數是周期序數的2倍,E的單質是黃綠色氣體;據此填空:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com