

分析 以硅孔雀石[主要成分為CuCO3•Cu(OH)2、CuSiO3•2H2O,含SiO2、FeCO3、Fe2O3等雜質]加入鹽酸酸浸生成二氧化碳氣體,過濾得到濾渣1為SiO2 ,H2SiO3,濾液中通入氯氣氧化亞鐵離子為鐵離子,加入氧化銅或氫氧化銅或堿式碳酸銅調節溶液PH沉淀鐵離子,過濾得到濾渣2為氫氧化鐵沉淀,濾液濃縮蒸發,冷卻結晶得到氯化銅晶體,加入SOCl2加熱脫水得到氯化銅,
(1)“酸浸”時鹽酸與CuCO3•Cu(OH)2反應為復分解反應,由此確定產物配平得化學方程式為CuCO3•Cu(OH)2+4HCl═2CuCl2+CO2↑+3H2O,升高溫度、加速攪拌、延長浸出時間等可以提高浸出率;
(2)硅孔雀石主要成分為CuCO3•Cu(OH)2、CuSiO3•2H2O,含SiO2、FeCO3、Fe2O3等雜質,根據流程圖,加鹽酸“酸浸”后溶液中只有Fe2+可被氯氣氧化,“氧化”時發生反應的離子方程式為Cl2+2Fe2+═2Fe3++2Cl-;
(3)根據流程圖,經氧化后溶液中陽離子主要為Cu2+和Fe3+,加試劑X調節pH使Fe3+完全沉淀而除去,Cu2+仍留在溶液中,實現Cu2+和Fe3+的分離,最終制備CuCl2;“調pH”時,pH不能過高,否則Cu2+轉化為Cu(OH)2沉淀;
(4)由已知:SOCl2+H2O$\frac{\underline{\;\;△\;\;}}{\;}$SO2↑+2HCl↑,“加熱脫水”時,加入SOCl2的目的是生成的HCl抑制CuCl2的水解.
解答 解:(1)“酸浸”時鹽酸與CuCO3•Cu(OH)2反應為復分解反應,由此確定產物配平得化學方程式為CuCO3•Cu(OH)2+4HCl═2CuCl2+CO2↑+3H2O,為提高“酸浸”時銅元素的浸出率,適當提高鹽酸濃度、適當提高反應溫度、適當加快攪拌速率、適當延長酸浸時間,
故答案為:CuCO3•Cu(OH)2+4HCl═2CuCl2+CO2↑+3H2O;適當提高鹽酸濃度、適當提高反應溫度、適當加快攪拌速率、適當延長酸浸時間;
(2)硅孔雀石主要成分為CuCO3•Cu(OH)2、CuSiO3•2H2O,含SiO2、FeCO3、Fe2O3等雜質,根據流程圖,加鹽酸“酸浸”后溶液中只有Fe2+可被氯氣氧化,“氧化”時發生反應的離子方程式為Cl2+2Fe2+═2Fe3++2Cl-,
故答案為:Cl2+2Fe2+═2Fe3++2Cl-;
(3)根據流程圖,經氧化后溶液中陽離子主要為Cu2+和Fe3+,加試劑X調節pH使Fe3+完全沉淀而除去,Cu2+仍留在溶液中,實現Cu2+和Fe3+的分離,最終制備CuCl2;“調pH”時,pH不能過高,否則Cu2+轉化為Cu(OH)2沉淀,
故答案為:Fe(OH)3 ;防止Cu2+轉化為Cu(OH)2沉淀;
(4)由已知:SOCl2+H2O$\frac{\underline{\;\;△\;\;}}{\;}$SO2↑+2HCl↑,“加熱脫水”時,加入SOCl2的目的是生成的HCl抑制CuCl2的水解.
故答案為:生成的HCl抑制CuCl2的水解.
點評 本題借助硅孔雀石為原料制取硫酸銅的工藝流程,考查了化學方程式書寫、氧化還原反應等知識,可以根據所學知識完成,題目難度中等.


科目:高中化學 來源: 題型:解答題
 研究NO2、SO2、CO等大氣污染氣體的處理具有重要意義.
研究NO2、SO2、CO等大氣污染氣體的處理具有重要意義.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Na+、Fe3+、K+、ClO- 都可在該物質的溶液中大量共存 | |
| B. | 檢驗該物質中Fe2+是否變質的方法是向該物質的溶液中滴入幾滴KSCN溶液,觀察溶液是否變紅色 | |
| C. | 向0.1mol•L-1該物質的溶液中逐滴滴加0.1mol•L-1NaOH溶液,生成沉淀的物質的量與加入NaOH溶液體積的關系如上圖所示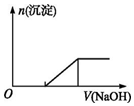 | |
| D. | 向該物質的溶液中滴加Ba(OH)2溶液,恰好使SO42-完全沉淀的離子方程式為:Fe2++2SO42-+2Ba2++2OH-═2BaSO4↓+Fe(OH)2↓ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com